张运召医生的科普号
- 精选 膀胱癌诊断治疗指南
目录一、前言二、膀胱癌的流行病学和病因学三、膀胱癌的组织病理学四、膀胱癌的诊断五、非肌层浸润性膀胱癌的治疗六、肌层浸润性膀胱癌的治疗七、尿流改道术八、膀胱癌的化疗与放疗九、膀胱癌患者的生活质量、预后与随访十、膀胱非尿路上皮癌一、前言膀胱癌是我国泌尿外科临床上最常见的肿瘤之一,是一种直接威胁患者生存的疾病。为了进一步规范膀胱癌诊断和治疗方法的选择,提高我国膀胱癌的诊断治疗水平,中华医学会泌尿外科学分会于2006年组织有关专家组成编写组,在学会委员会的直接领导与组织下,以国内外循证医学资料为依据,参考《吴阶平泌尿外科学》、Campbell’s Urology以及欧洲泌尿外科学会(EAU)、美国泌尿外科学会(AUA)、美国国立综合癌症网络(NCCN)等相关膀胱癌诊断治疗指南,结合国内临床实际,编写完成了2007年版中国《膀胱癌诊断治疗指南》,并在2009年进行了更新,为我国不同医疗条件下泌尿外科医师选择合理的膀胱癌诊断方法与治疗手段提供了有益的指导,对提高我国膀胱癌的诊治水平起到了巨大的推动作用。两年来,随着膀胱癌诊断治疗相关研究的进展,使得《膀胱癌诊断治疗指南》又有了进一步更新的需要。在中华医学会泌尿外科学分会的统一领导安排下,《膀胱癌诊断治疗指南》编写组通过广泛征求意见,仔细查阅最新相关文献,并经过反复讨论,完成此版更新后的《膀胱癌诊断治疗指南》,以期对膀胱癌的临床诊断治疗工作提供更好的帮助。本版《膀胱癌诊断治疗指南》中共引用371条文献,其中由我国学者在国内或国际学术期刊中发表的论文共35条。二、膀胱癌的流行病学和病因学(一)流行病学1.发病率和死亡率 世界范围内,膀胱癌发病率居恶性肿瘤的第九位,在男性排名第六位,女性排在第十位之后。在欧美,膀胱癌发病率居男性恶性肿瘤的第四位,位列前列腺癌、肺癌和结肠癌之后,在女性恶性肿瘤亦排在十位以后。2002年世界膀胱癌年龄标准化发病率男性为10.1/10万,女性为2.5/10万,年龄标准化死亡率男性为4/10万,女性为1.1/10万。美国男性膀胱癌发病率为24.1/10万,女性为6.4/10万。美国癌症协会预测2010年美国膀胱癌新发病例数为70530例(男52760例,女17770例),死亡病例数为14680例(男10410例,女4270例)。在我国,男性膀胱癌发病率位居全身肿瘤的第八位,女性排在第十二位以后,发病率远低于西方国家,2002年我国膀胱癌年龄标准化发病率男性为3.8/10万,女性为1.4/10万。近年来,我国部分城市肿瘤发病率报告显示膀胱癌发病率有增高趋势。膀胱癌男性发病率为女性的3-4倍。且城市居民膀胱癌死亡率明显高于农村。2009年我国城市居民膀胱癌年龄标准化死亡率男性为3.79/10万,女性为1.30/10万;而农村男性居民膀胱癌年龄标准化死亡率为2.42/10万,女性为0.81/10万[8]。而对分期相同的膀胱癌,女性的预后比男性差。男性膀胱癌发病率高于女性不能完全解释为吸烟习惯和职业因素,性激素可能是导致这一结果的重要原因。膀胱癌可发生在任何年龄,甚至于儿童。但是主要发病年龄在中年以后,并且其发病率随年龄增长而增加。2001-2005年,美国65岁以下男性膀胱癌发病率为9.5/10万,女性为2.9/10万;而65岁以上老年男性发病率则为229.4/10万,女性为54.3/10万。种族对膀胱癌发病的影响迄今还没有确定。美国黑人膀胱癌发病危险率为美国白人的一半,但是其总体生存率却更差,而美国白人发病率高于美国黑人仅局限于非肌层浸润性肿瘤,而肌层浸润性膀胱癌的发病危险率却相似。由于对低级别肿瘤认识不同,不同国家报道的膀胱癌发病率存在差异,使不同地域间的比较非常困难。不同人群的膀胱癌组织类型不同,在美国及大多数国家中,以移行细胞癌为主,占膀胱癌的90%以上,而非洲国家则以血吸虫感染所致的鳞状细胞癌为主,如在埃及,鳞状细胞癌约占膀胱癌的75%。2.自然病程 大部分膀胱癌患者确诊时处于分化良好或中等分化的非肌层浸润性膀胱癌,其中约10%的患者最终发展为肌层浸润性膀胱癌或转移性膀胱癌。膀胱癌的大小、数目、分期与分级与其进展密切相关,尤其是分期与分级,低分期低分级肿瘤发生疾病进展的风险低于高分期高分级肿瘤。总体上说,T1期膀胱癌发生肌肉浸润的风险要远高于Ta期。在欧洲肿瘤协作组(EORTC)广泛采用的用于预测膀胱癌复发及进展的权重评分表中,Ta期膀胱癌发生进展的权重评分为0,而T1期进展的权重评分则为4。但膀胱癌的分级可能是更为重要的预测因子。研究发现:G1级膀胱癌出现进展的风险(6%)仅为G3级膀胱癌(30%)的1/5。一组长达20年的随访资料发现,G3级膀胱癌出现疾病进展风险更高,TaG1膀胱癌为14%,而T1G3则高达45%,但是其复发的风险却相同,约为50%。原位癌的发病率占非肌层浸润性膀胱癌的5%-10%,Lamm将原位癌分为3型。Ⅰ型没有侵袭性,单一病灶,为疾病的早期阶段。Ⅱ型为多病灶,可引起膀胱刺激症状。Ⅲ型合并有一个或多个其他膀胱癌,会增加肿瘤复发、进展及死亡的风险。经腔内切除的Ⅱ型原位癌发生疾病进展的风险约54%,膀胱灌注化疗可降低其进展风险至30%-52%,而BCG膀胱灌注可以将风险降至30%以下。(二)致病的危险因素与病因学膀胱癌的发生是复杂、多因素、多步骤的病理变化过程,既有内在的遗传因素,又有外在的环境因素。较为明确的两大致病危险因素是吸烟和长期接触工业化学产品。吸烟是目前最为肯定的膀胱癌致病危险因素,约30%-50%的膀胱癌由吸烟引起,吸烟可使膀胱癌危险率增加2-4倍,其危险率与吸烟强度和时间成正比。另一重要的致病危险因素为长期接触工业化学产品,职业因素是最早获知的膀胱癌致病危险因素,约20%的膀胱癌是由职业因素引起的,包括从事纺织、染料制造、橡胶化学、药物制剂和杀虫剂生产、油漆、皮革及铝、铁和钢生产。柴油机废气累积也可增加膀胱癌的发生危险。其他可能的致病因素还包括慢性感染(细菌、血吸虫及HPV感染等)、应用化疗药物环磷酰胺(潜伏期6-13年)、滥用含有非那西汀的止痛药(10年以上)、近期及远期的盆腔放疗史、长期饮用砷含量高的水和氯消毒水、咖啡、人造甜味剂及染发。另外,膀胱癌还可能与遗传有关,有家族史者发生膀胱癌的危险性明显增加,遗传性视网膜母细胞瘤患者的膀胱癌发生率也明显升高。对于肌层浸润性膀胱癌,慢性尿路感染、残余尿及长期异物刺激(留置导尿管、结石)与之关系密切,其主要见于鳞状细胞癌和腺癌。正常膀胱细胞恶变开始于细胞DNA的改变。流行病学证据表明化学致癌物是膀胱癌的致病因素,尤其是芳香胺类化合物,如2-萘胺、4-氨基联苯,广泛存在于烟草和各种化学工业中。烟草代谢产物经尿液排出体外,尿液中的致癌成分诱导膀胱上皮细胞恶变。目前大多数膀胱癌病因学研究集中在基因改变。癌基因是原癌基因的突变形式,原癌基因编码正常细胞生长所必须的生长因子和受体蛋白。原癌基因突变后变为癌基因,可使细胞无节制的分裂,导致膀胱癌复发和进展。与膀胱癌相关的癌基因包括HER-2、H-Ras、BcL-2、FGFR3、C-myc、c-erbB-2、MDM2、CDC91L1等。膀胱癌发生的另一个重要分子机制是编码调节细胞生长、DNA修复或凋亡的蛋白抑癌基因失活,使DNA受损的细胞不发生凋亡,导致细胞生长失控。研究发现:含有p53、Rb、p21等抑癌基因的17、13、9号染色体的缺失或杂合性丢失与膀胱癌的发生发展密切相关,而且,P53、Rb的突变或失活也与膀胱癌侵袭力及预后密切相关。近来,SYK、CAGE-1等基因的超甲基化被认为与膀胱癌的进展相关。此外,膀胱癌的发生还包括编码生长因子或其受体的正常基因的扩增或过表达,如EGFR过表达可增加膀胱癌的侵袭力及转移。尿路上皮肿瘤具有时间和空间的多中心性,上尿路尿路上皮肿瘤的病史是膀胱尿路上皮癌的重要危险因素,研究表明,上尿路尿路上皮癌治疗后出现膀胱癌的风险累计达15%-50%,但目前尚无可靠的指标对膀胱癌的发病风险进行预测。三、膀胱癌的组织病理学目前,膀胱癌的分级广泛采用WHO的国际肿瘤组织学分类(WHO 1973, 1998, 2004)分级标准,而浸润深度则主要以国际抗癌联盟 (Union Internationale Contre le Cancer/International Union Against Cancer, UICC) TNM分期法为标准。(一)膀胱癌的组织学类型被覆尿路的上皮统称为尿路上皮(urothelium)或移行上皮(transitional epithelium),本指南中主要采用尿路上皮的概念。膀胱癌包括尿路上皮(移行)细胞癌、鳞状细胞癌和腺细胞癌,其次还有较少见的小细胞癌、混合型癌、癌肉瘤及转移性癌等。其中,膀胱尿路上皮癌最为常见,占膀胱癌的90%以上;膀胱鳞状细胞癌比较少见,约占膀胱癌的3%~7%。膀胱腺癌更为少见,占膀胱癌的比例<2% ,膀胱腺癌是膀胱外翻最常见的癌。(二)膀胱癌的组织学分级膀胱癌的分级与膀胱癌的复发和侵袭行为密切相关。膀胱肿瘤的恶性程度以分级(Grade)表示。关于膀胱癌的分级,目前普遍采用WHO分级法(WHO 1973, WHO/ISUP 1998, WHO2004)。1. WHO1973分级法 1973年的膀胱癌组织学分级法根据癌细胞的分化程度分为高分化、中分化和低分化3级,分别用grade 1、2、3或grade Ⅰ、Ⅱ、Ⅲ表示 (表1)。2. WHO/ISUP分级法:1998年WHO和国际泌尿病理协会 ( International Society of Urological Pathology, ISUP) 提出了非浸润性尿路上皮(移行细胞)癌新分类法,2004年WHO正式公布了这一新的分级法。此分级法将尿路上皮肿瘤分为低度恶性倾向尿路上皮乳头状肿瘤(papillary urothelial neoplasms of low malignant potential, PUNLMP)、低分级和高分级尿路上皮癌 (表1) (www.pathology.jhu.edu/bladder上可以查到各级膀胱肿瘤的详细描述)。低度恶性倾向尿路上皮乳头状肿瘤的定义为尿路上皮乳头状肿瘤,其细胞形态正常,无恶性肿瘤的细胞学特征。虽然,此种尿路上皮肿瘤进展的风险很小,但不完全属于良性病变,仍有复发的可能。建议使用WHO 2004分级法,以便用统一的标准诊断膀胱肿瘤,更好地反映肿瘤的危险倾向。但是,需要更多的临床试验验证新的WHO分级法优于WHO 1973分级法。目前应该同时使用WHO 1973,WHO 2004分级标准。(三)膀胱癌的分期膀胱癌的分期指肿瘤浸润深度及转移情况,是判断膀胱肿瘤预后的最有价值的参数。国际抗癌协会的2002年第6版TNM分期法已被普遍采用,2009年更新为第7版(表2),其中膀胱癌的T分期和M分期较过去的2002年第6版没有变化,N-淋巴结分期进行了重新修订,不再以淋巴结大小作为淋巴结分期的依据。膀胱癌可分为非肌层浸润性膀胱癌(Tis, Ta, T1)和肌层浸润性膀胱癌(T2以上)。原位癌虽然也属于非肌层浸润性膀胱癌,但一般分化差,属于高度恶性的肿瘤,向肌层浸润性进展的几率要高得多。因此,应将原位癌与Ta、T1期膀胱癌加以区别。推荐意见:1. 膀胱癌分期系统 推荐采用膀胱癌2009 TNM分期系统(UICC)。2. 膀胱癌分级系统 在证明新的WHO分级法比WHO 1973分级法更合理之前,应该同时使用WHO 1973和WHO 2004分级法。四、膀胱癌的诊断(一)早期检测与症状血尿是膀胱癌最常见的症状,尤其是间歇全程无痛性血尿,可表现为肉眼血尿或镜下血尿,血尿出现时间及出血量与肿瘤恶性程度、分期、大小、数目、形态并不一致。膀胱癌患者亦有以尿频、尿急、排尿困难和盆腔疼痛为首发表现,为膀胱癌另一类常见的症状,常与弥漫性原位癌或浸润性膀胱癌有关[1],而Ta、T1期肿瘤无此类症状。其他症状还包括输尿管梗阻所致腰胁部疼痛、下肢水肿、盆腔包块、尿潴留。有的患者就诊时即表现为体重减轻、肾功能不全、腹痛或骨痛,均为晚期症状。(二)体格检查膀胱癌患者触及盆腔包块多是局部进展性肿瘤的证据。体检还包括经直肠、经阴道指检和麻醉下腹部双合诊等,但体检在Ta、T1期膀胱癌中的诊断价值有限。 (三)影像学检查1.超声检查 超声检查可通过三种途径(经腹、经直肠、经尿道)进行,可同时检查肾脏、输尿管、前列腺和其他脏器(如肝脏等)。经直肠超声显示膀胱三角区、膀胱颈和前列腺较清楚。经尿道超声应用不太广泛,需麻醉,但影像清晰,分期准确性较高。国外报道经尿道超声判定肿瘤分期,与病理分期相比,结果显示非肌层浸润性肿瘤准确率为94%~100%,肌层浸润性肿瘤准确率为63%~96.8%。彩色多普勒超声检查还可显示肿瘤基底部血流信号,但膀胱肿瘤血流征象对术前肿瘤分期、分级帮助不大。总之,超声检查不仅可以发现膀胱癌,还有助于膀胱癌分期,了解有无局部淋巴结转移及周围脏器侵犯,尤其适用于造影剂过敏者[2]。2. 泌尿系统平片和静脉尿路造影(KUB+IVU) 泌尿系统平片及静脉尿路造影检查一直被视为膀胱癌患者的常规检查,以期发现并存的上尿路肿瘤。但初步诊断时此项检查的必要性目前受到置疑,因为其获得的重要信息量较少。泌尿系统CT成像(CTU)可替代传统IVU检查, 可提供更多的检查信息,并对泌尿上皮肿瘤具有更高的诊断准确率,而缺点是更多的射线暴露量。一组793例膀胱肿瘤患者上尿路肿瘤发生率仅有1.1%(9例),而IVU只对6例做出诊断。但如果怀疑有T1G3肿瘤(该类肿瘤可致上尿路肿瘤发生率增加7%)、浸润性膀胱肿瘤或膀胱肿瘤并发肾盂、输尿管肿瘤以及有肾积水征象时仍有其应用价值。3. CT检查 传统CT(平扫+增强扫描)对诊断膀胱肿瘤有一定价值,可发现较大肿瘤,还可与血块鉴别。近年来,多排(64~128排)螺旋CT分辨率大大提高,可以发现较小肿瘤(1~5mm),但是原位癌仍不易被发现,不能了解输尿管情况,分期准确性不高,肿大淋巴结不能区分是转移还是炎症,不能准确区分肿瘤是局限于膀胱还是侵犯到膀胱外,而且既往有肿瘤切除史者可因局部炎症反应所致的假象而造成分期过高。因此,如果膀胱镜发现肿瘤为实质性(无蒂)、有浸润到肌层的可能或了解肝脏有无病变时可进行CT检查。一组浸润性膀胱肿瘤患者行CT检查,诊断准确率只有54.9%,39%分期偏低,6.1%偏高。但患者若存在尿道狭窄或膀胱有活动性出血不能进行膀胱镜检查,CT仍有其优越性。CT仿真膀胱镜可获取与膀胱镜相似的视觉信息,虽不能完全替代膀胱镜,但有其应用价值,是膀胱镜较好的替代和补充方法。施行CT仿真膀胱镜时,一种方法是将尿液引出,用气体充盈膀胱,然后进行扫描,将所获数据进行三维重建。采用CT仿真膀胱镜检查准确率为88%,CT仿真膀胱镜对>5 mm的肿块能准确识别,并可以显示小至2mm的粘膜异常。CT仿真膀胱镜检查还可经静脉或经膀胱注入造影剂进行对比。国内一项研究对膀胱癌患者行螺旋CT多平面重组(MPR)、三维(3D)重建和CT仿真膀胱镜(CTVC)成像,结果显示CT对肿瘤术前分期准确率为87.7%,轴位图像能较好显示浸润深度。MPR可更直观观察肿瘤起源、向周围侵犯情况及其与输尿管的关系。3D和CTVC能清楚显示肿瘤大体形态及其与输尿管开口的关系。4. 胸部检查 术前应常规拍胸部X线片,了解有无肺部转移。对肺部转移最敏感的检查方法是胸部CT 。5. MRI检查 传统MRI对膀胱癌检查并无明显优越之处。MRI检查膀胱,T1加权像尿呈极低信号,膀胱壁为低至中度信号,而膀胱周围脂肪为高信号。T1加权像有助于检查扩散至邻近脂肪的肿瘤、淋巴结转移以及骨转移情况,甚至可评价除前列腺以外的邻近器官受侵犯情况。T2加权像尿液呈高信号,正常逼尿肌呈低信号,而大多数膀胱癌为中等信号。低信号的逼尿肌下方的肿瘤出现中断现象提示肌层浸润。因此,MRI有助于肿瘤分期。动态MRI在显示是否有尿路上皮癌存在以及肌层侵犯程度方面准确性高于CT或非增强MRI [19]。由于膀胱肿瘤的平均表观弥散系数(ADC)较周围组织低,弥散加权成像(DWI)能更好的对肿瘤的T分期进行术前评估,且在可能在评估肿瘤侵犯周围组织中有价值。应用MRI仿真膀胱镜诊断肿瘤效果较好(包括较小肿瘤)。膀胱癌患者行MRI膀胱造影,以术中或膀胱镜结果作为参考标准,仿真膀胱镜重建与多维重建的敏感性和特异性较高。在分期方面,应用增强剂行MRI检查进行分期,可区分非肌层浸润性肿瘤与肌层浸润性肿瘤以及浸润深度,也可发现正常大小淋巴结有无转移征象。例如,应用铁剂作为增强剂可鉴别淋巴结有无转移:良性增大的淋巴结可吞噬铁剂,在T2加权像上信号强度降低,而淋巴结转移则无此征象。最近有人评价钆增强MRI对膀胱癌分期的准确程度,MRI分期准确率为62%,32%出现分期过高,但在区分非肌层浸润性肿瘤与肌层浸润性肿瘤或区分肿瘤局限于膀胱与否方面,MRI分期准确率则分别提高到85%和82%。在检测有无骨转移时MRI敏感性远高于CT,甚至高于核素骨扫描。6. 骨扫描 一般不做常规使用。只在浸润性肿瘤患者出现骨痛,怀疑有骨转移时使用。7. PET(正电子发射断层扫描)一般不用于诊断,因示踪剂FDG(氟脱氧葡萄糖)经肾脏排泌入膀胱会影响对较小肿瘤的诊断,而且费用较高,限制了其应用。目前,PET/CT主要应用于肌层浸润性膀胱癌术前分期,但有关肿瘤分期目前研究较少,例数不多,因而结果也不甚相同。尽管已有使用新型示踪剂(如胆碱、蛋氨酸)的报道,有限的数据显示11C-胆碱可能是检测淋巴结转移的一种很有前途的示踪剂,但还需进一步证实。(四)尿细胞学尿细胞学检查是膀胱癌诊断和术后随诊的主要方法之一。尿标本的采集一般是通过自然排尿,也可以通过膀胱冲洗,这样能得到更多的癌细胞,利于提高诊断率。尿细胞学阳性意味着泌尿道的任何部分,包括:肾盏、肾盂、输尿管、膀胱和尿道,存在尿路上皮癌的可能。根据文献报道,尿细胞学检测膀胱癌的敏感性为13%~75%,特异性为85%~100%。敏感性与癌细胞恶性分级密切相关,分级低的膀胱癌敏感性较低,一方面是由于肿瘤细胞分化较好,其特征与正常细胞相似,不易鉴别,另一方面由于癌细胞之间黏结相对紧密,没有足够多的癌细胞脱落到尿中而被检测到,所以尿细胞学阴性并不能排除低级别尿路上皮癌的存在;相反,分级高的膀胱癌或原位癌,敏感性和特异性均较高。尿标本中癌细胞数量少、细胞的不典型或退行性变、泌尿系感染、结石、膀胱灌注治疗和检查者的技术差异等因素会影响尿细胞学检查结果[33, 34]。(五)尿液膀胱癌标记物为了提高无创检测膀胱癌的水平,尿液膀胱癌标记物的研究受到了很大的关注,美国FDA已经批准将BTAstat、BTAtrak、NMP22、FDP、ImmunoCyt和FISH用于膀胱癌的检测。其他还有许多的标记物,如:端粒酶、存活素 (survivin)、微卫星分析、CYFRA21-1和LewisX等,在检测膀胱癌的临床研究中显示了较高的敏感性和特异性。虽然大部分尿液膀胱癌标记物显示出了较高的敏感性,但是其特异性却普遍低于尿细胞学检查,到目前为止,仍然没有一种理想的标记物能够取代膀胱镜和尿细胞学检查而对膀胱癌的诊断、治疗、术后随诊和预后等方面做出足够的判断。相信随着新技术的出现,尿液膀胱癌标记物的研究和应用前景是光明的。(六)膀胱镜检查和活检膀胱镜检查和活检是诊断膀胱癌最可靠的方法。通过膀胱镜检查可以明确膀胱肿瘤的数目、大小、形态(乳头状的或广基的)、部位以及周围膀胱粘膜的异常情况,同时可以对肿瘤和可疑病变进行活检以明确病理诊断。如有条件,建议使用软性膀胱镜检查,与硬性膀胱镜相比,该方法具有损伤小、视野无盲区、相对舒适等优点。膀胱肿瘤通常是多灶性的,非肌层浸润性膀胱癌可以伴有原位癌或发育不良,表现为类似炎症的淡红色绒毛样的粘膜改变,也可以完全表现为正常。不建议对非肌层浸润性膀胱癌的正常膀胱粘膜实行常规的随机活检或选择性活检,因为发现原位癌的可能性很低(小于2%),特别是对于那些低风险的膀胱癌。但当尿脱落细胞学检查阳性或膀胱粘膜表现异常时,建议行选择性活检(selected biopsy),以明确诊断和了解肿瘤范围。在尿细胞学检查阳性而膀胱粘膜表现为正常、怀疑有原位癌存在时,应考虑行随机活检。如果膀胱肿瘤为原位癌、多发性癌或者肿瘤位于膀胱三角区或颈部时,并发前列腺部尿道癌的危险性增加,建议行前列腺部尿道活检,此外,尿细胞学阳性或前列腺部尿道粘膜表现异常时,也应行该部位的活检。(七)诊断性经尿道电切术(TUR)如果影像学检查发现膀胱内有非肌层浸润的肿瘤占位病变,可以省略膀胱镜检查,直接行TUR,这样可以达到两个目的,一是切除肿瘤,二是明确肿瘤的病理诊断和分级、分期,为进一步治疗以及判断预后提供依据。TUR方法:如果肿瘤较小(小于1cm),可以将肿瘤与其基底的部分膀胱壁一起切除送病理检查;如果肿瘤较大,则行分步骤切除,先将肿瘤的突起部分切除,然后切除肿瘤的基底部分,基底部分应包含膀胱壁肌层,最后切除肿瘤的周边区域,将这三部分标本分别送病理检查 。TUR时尽量避免烧灼,以减少对标本组织的破坏。(也可以使用活检钳对肿瘤基底部以及周围粘膜进行活检,这样能够有效地保护标本组织不受损伤,可以配合TUR酌情使用。)(八)荧光膀胱镜检查荧光膀胱镜检查是通过向膀胱内灌注光敏剂,如:5-氨基酮戊酸(5-ALA)、Hexaminolaevulinate(HAL)或Hypericin,产生的荧光物质能高选择的积累在新生的膀胱粘膜组织中,在激光激发下病灶部位显示为红色荧光,与正常膀胱粘膜的蓝色荧光形成鲜明对比,能够发现普通膀胱镜难以发现的小肿瘤、发育不良或原位癌,检出率可以提高14%~25%。欧洲泌尿外科学会指南推荐,在怀疑有膀胱原位癌或尿细胞学检查阳性而普通膀胱镜检查正常时,应该考虑使用荧光膀胱镜做进一步检查。近来有报道,在荧光膀胱镜引导下行膀胱肿瘤电切术,与普通的电切术相比,能够明显降低肿瘤的术后复发率,但对肿瘤的进展率和患者生存率的影响还有待于做进一步的临床观察[50]。荧光膀胱镜的缺点是诊断膀胱癌的特异性相对不高,炎症、近期膀胱肿瘤电切术和膀胱灌注治疗会导致假阳性结果。(九)二次经尿道电切术(ReTUR)非肌层浸润性膀胱癌电切术后,相当多的肿瘤复发是由于肿瘤残余造成的,特别是中、高分级的T1期膀胱癌,首次电切术后肿瘤残余率可以达到33.8%~36%,此外,由于电切技术和送检肿瘤标本质量问题,首次电切还可以造成一部分肿瘤的病理分期偏差。一些学者建议,对非肌层浸润性膀胱癌在首次电切术后短期内进行ReTUR,特别是对那些高风险的T1期膀胱癌,可以降低术后肿瘤复发率和进展率,并且可以获得更准确的肿瘤病理分期。文献报道,ReTUR可以使T1期膀胱癌患者术后的肿瘤复发率由63.24%降到25.68%,肿瘤进展率由11.76%降到4.05%。至于首次电切术后何时进行ReTUR目前还没有定论,多数学者建议在首次电切术后2~6周内进行。推荐意见:1.膀胱肿瘤患者需询问病史,做体格检查、尿常规、B超、尿脱落细胞学、IVU检查及胸部X线片。2.对所有考虑膀胱癌的患者应行膀胱镜检查及病理活检或诊断性TUR。3.对怀疑原位癌、尿脱落细胞学阳性而无明确粘膜异常者应考虑随机活检。4.对肌层浸润性膀胱癌患者根据需要可选择盆腔CT/MRI、骨扫描。五、非肌层浸润性膀胱癌的治疗非肌层浸润性膀胱癌(non muscle-invasive bladder cancer)或表浅性膀胱癌(superficial bladder cancer)占初发膀胱肿瘤的70%,其中Ta占70%、T1占20%、Tis占10%。Ta和T1虽然都属于非肌层浸润性膀胱癌,但两者的生物学特性有显著不同,由于固有层内血管和淋巴管丰富,故 T1容易发生肿瘤扩散。某些因素同非肌层浸润性膀胱癌的预后密切相关。其中与复发密切相关的因素包括肿瘤数目、肿瘤的复发频率,尤其是术后3个月时有无复发、肿瘤大小、肿瘤分级。与肿瘤进展最相关的因素包括肿瘤的病理分级和肿瘤分期。膀胱颈处的肿瘤预后较差。根据复发风险及预后的不同,非肌层浸润性膀胱癌可分为以下三组:1. 低危非肌层浸润性膀胱尿路上皮癌 单发、Ta、G1(低级别尿路上皮癌)、直径<3cm(注:必须同时具备以上条件才是低危非肌层浸润性膀胱癌)。2. 高危非肌层浸润性膀胱尿路上皮癌 多发或高复发、T1、G3(高级别尿路上皮癌)、Tis。3. 中危非肌层浸润性膀胱尿路上皮癌 除以上两类的其他情况,包括肿瘤多发、Ta~T1、 G1~G2(低级别尿路上皮癌)、直径>3cm等。欧洲膀胱癌指南根据EORTC评分表的肿瘤评分,将非肌层浸润性膀胱尿路上皮癌分为低危、中危和高危(参见九(二)《膀胱癌的预后因素》一节)。(一)手术治疗1.经尿道膀胱肿瘤切除术 经尿道膀胱肿瘤切除术(TUR-BT)既是非肌层浸润性膀胱癌的重要诊断方法,同时也是主要的治疗手段。膀胱肿瘤的确切病理分级、分期都需要借助首次TUR-BT后的病理结果获得[9,10]。经尿道膀胱肿瘤切除术有两个目的:一是切除肉眼可见的全部肿瘤,二是切除组织进行病理分级和分期。TUR-BT术应将肿瘤完全切除直至露出正常的膀胱壁肌层。肿瘤切除后,建议进行基底部组织活检,便于病理分期和下一步治疗方案的确定。对于肿瘤切除不完全、标本内无肌层、高级别肿瘤和T1期肿瘤,建议术后2~6周再次行TUR-BT,可以降低术后复发概率。2.经尿道激光手术 激光手术可以凝固,也可以汽化,其疗效及复发率与经尿道手术相近。但术前需进行肿瘤活检以便进行病理诊断。激光手术对于肿瘤分期有困难,一般适合于乳头状低级别尿路上皮癌,以及病史为低级别、低分期的尿路上皮癌。3.光动力学治疗 光动力学治疗(photodynamic therapy, PDT)是利用膀胱镜将激光与光敏剂相结合的治疗方法。肿瘤细胞摄取光敏剂后,在激光作用下产生单态氧,使肿瘤细胞变性坏死。膀胱原位癌、控制膀胱肿瘤出血、肿瘤多次复发、不能耐受手术治疗等情况可以选择此疗法。(二)术后辅助治疗1.术后膀胱灌注化疗 TUR-BT术后有10%~67%的患者会在12个月内复发,术后5年内有24%~84%的患者复发,可能与新发肿瘤、肿瘤细胞种植或原发肿瘤切除不完全有关。非肌层浸润性膀胱癌TUR-BT术后复发有两个高峰期,分别为术后的100~200天和术后的600天。术后复发的第一个高峰期同术中肿瘤细胞播散有关,而术后膀胱灌注治疗可以大大降低由于肿瘤细胞播散而引起的复发。尽管在理论上TUR-BT术可以完全切除非肌层浸润的膀胱癌,但在临床治疗中仍有很高的复发概率,而且有些病例会发展为肌层浸润性膀胱癌。单纯TUR-BT术不能解决术后高复发和进展问题,因此建议所有的非肌层浸润性膀胱癌患者术后均进行辅助性膀胱灌注治疗。(1)TUR-BT术后即刻膀胱灌注化疗:TUR-BT术后24小时内完成表柔比星(epirubicin)、吡柔比星(THP)或丝裂霉素(mitomycin)等膀胱灌注化疗可以使肿瘤复发率降低39%,因此推荐所有的非肌层浸润性膀胱癌患者TUR-BT术后24小时内均进行膀胱灌注化疗,但术中有膀胱穿孔或术后明显血尿时不宜采用。TUR-BT术后即刻膀胱灌注化疗对单发和多发膀胱癌均有效。低危非肌层浸润性膀胱癌术后即刻灌注后,肿瘤复发的概率很低,因此即刻灌注后可以不再继续进行膀胱灌注治疗。(2)术后早期膀胱灌注化疗及维持膀胱灌注化疗:对于中危和高危的非肌层浸润性膀胱癌,术后24小时内即刻膀胱灌注治疗后,建议继续膀胱灌注化疗,每周1次,共4~8周,随后进行膀胱维持灌注化疗,每月1次,共6~12个月。研究显示,非肌层浸润性膀胱癌维持灌注治疗6个月以上时不能继续降低肿瘤的复发概率,因此建议术后维持膀胱灌注治疗6个月。但也有研究发现表柔比星维持灌注1年可以降低膀胱肿瘤的复发概率。灌注期间出现严重的膀胱刺激症状时,应延迟或停止灌注治疗,以免继发膀胱挛缩。膀胱灌注治疗的副作用与药物剂量和灌注频率有关。膀胱灌注治疗主要用于减少膀胱肿瘤的复发,没有证据显示其能预防肿瘤进展。(3)膀胱灌注化疗的药物:膀胱灌注化疗常用药物包括表柔比星、丝裂霉素、吡柔比星、阿霉素、羟基喜树碱等。尿液的pH值、化疗药的浓度与膀胱灌注化疗效果有关,并且药物浓度比药量更重要。化疗药物应通过导尿管灌入膀胱,并保留0.5~2小时 (注:膀胱内保留时间需依据药物说明书)。灌注前不要大量饮水,避免尿液将药物稀释。表柔比星的常用剂量为50~80mg,丝裂霉素为20~60mg,吡柔比星为30mg,羟基喜树碱为10~20mg。其他的化疗药物还包括吉西他滨等。膀胱灌注化疗的主要副作用是化学性膀胱炎,程度与灌注剂量和频率相关,TUR-BT术后即刻膀胱灌注更应注意药物的副作用。多数副作用在停止灌注后可以自行改善。 2.术后膀胱灌注免疫治疗(1)卡介苗(BCG):BCG膀胱灌注指征:BCG的确切作用机制尚不清楚,多数研究认为是通过免疫反应介导的。BCG适合于高危非肌层浸润性膀胱癌的治疗,可以预防膀胱肿瘤的进展。BCG不能改变低危非肌层浸润性膀胱癌的病程,而且由于BCG灌注的副作用发生率较高,对于低危非肌层浸润性膀胱尿路上皮癌不建议行BCG灌注治疗。对于中危非肌层浸润性膀胱尿路上皮癌而言,其术后5年肿瘤复发概率为42%~65%,而进展概率为5%~8%,因此,中危非肌层浸润膀胱尿路上皮癌膀胱灌注的主要目的是防止肿瘤复发,一般建议采用膀胱灌注化疗,某些情况也可以采用BCG灌注治疗。由于术后膀胱有创面,因此术后即刻灌注治疗应避免采用BCG,以免引起严重的副作用。BCG膀胱灌注的剂量:BCG治疗一般采用6周灌注诱导免疫应答,再加3周的灌注强化以维持良好的免疫反应。BCG灌注用于治疗高危非肌层浸润膀胱尿路上皮癌时,一般采用常规剂量(120~150mg);BCG用于预防非肌层浸润膀胱尿路上皮癌复发时,一般采用低剂量(60~75mg)。研究发现采用1/3剂量BCG灌注治疗中危非肌层浸润性膀胱尿路上皮癌时,其疗效与全剂量疗效相同,副作用却明显降低 。不同BCG菌株之间的疗效没有差别。BCG灌注一般在TUR-BT术后2周开始。BCG维持灌注可以使膀胱肿瘤进展概率降低37%。需维持BCG灌注1~3年(至少维持灌注1年),因此建议在3、6、12、18、24、36个月时重复BCG灌注,以保持和强化疗效[35,39]。BCG膀胱灌注的主要副作用为膀胱刺激症状和全身流感样症状,少见的副作用包括结核败血症、前列腺炎、附睾炎、肝炎等[39]。因此,TUR-BT术后膀胱有开放创面或有肉眼血尿等情况下,不能进行BCG膀胱灌注。(2)免疫调节剂:一些免疫调节剂与化疗药物一样可以预防膀胱肿瘤的复发,包括干扰素、钥孔戚血蓝素(keyhole limpet hemocyanin, KLH)等。3.复发肿瘤的灌注治疗 膀胱肿瘤复发后,一般建议再次TUR-BT治疗。依照TUR-BT术后分级及分期,按上述方案重新进行膀胱灌注治疗。对频繁复发和多发者,建议行BCG灌注治疗[。4.膀胱原位癌的治疗 膀胱原位癌的治疗方案是行彻底的TUR-BT术,术后行BCG膀胱灌注治疗。BCG灌注每周1次,每6周为1个周期,1个周期后有70%完全缓解。休息6周后,进行膀胱镜检和尿脱落细胞学检查,结果阳性者再进行1个周期,共6周的灌注治疗。另有15%的病例获得缓解。休息6周后,重复膀胱镜检和尿脱落细胞学检查,若结果仍为阳性,建议行膀胱根治性切除术及尿道根治性切除术。对于缓解的病例,应在第3、6、12、18、24、30和36个月时进行1个周期的BCG灌注防止复发。BCG治疗缓解率83%~93%,有11%~21%在5~7年内死于该病。无效及不完全反应肿瘤进展率33%~67%。若治疗9个月时未完全缓解或肿瘤复发,则建议行根治性膀胱切除术 。5.T1G3膀胱癌的治疗 T1G3膀胱癌通过BCG灌注治疗或膀胱灌注化疗,有50%可以保留膀胱。建议先行TUR-BT术,术后2~6周后再次行TUR-BT术。无肌层浸润者,术后行BCG灌注治疗或膀胱灌注化疗。对于2周期BCG灌注治疗或6个月膀胱灌注化疗无效或复发的病例,建议行根治性膀胱切除术。推荐意见:1. TUR-BT术是非肌层浸润性膀胱尿路上皮癌的主要治疗手段。2. 对低危非肌层浸润性膀胱尿路上皮癌,术后可只进行单剂即刻膀胱灌注化疗。3. 对中、高危非肌层浸润性膀胱尿路上皮癌,术后单剂即刻膀胱灌注化疗后,应进行后续化疗药物或BCG维持灌注治疗。4. 对高危非肌层浸润性膀胱尿路上皮癌,首选BCG膀胱灌注治疗(至少维持1年)。5.膀胱灌注治疗无效的非肌层浸润性膀胱尿路上皮癌(如肿瘤进展、肿瘤多次复发、 Tis和T1G3肿瘤经TUR-BT及膀胱灌注治疗无效等),则建议行根治性膀胱切除术。六、肌层浸润性膀胱癌的治疗(一)根治性膀胱切除术根治性膀胱切除术同时行盆腔淋巴结清扫术,是肌层浸润性膀胱癌的标准治疗,是提高浸润性膀胱癌患者生存率、避免局部复发和远处转移的有效治疗方法。该手术需要根据肿瘤的病理类型、分期、分级、肿瘤发生部位、有无累及邻近器官等情况,结合患者的全身状况进行选择。文献报道浸润性膀胱癌患者盆腔淋巴结转移的可能性为24%~43%,淋巴结清扫范围可根据肿瘤范围、病理类型、浸润深度和患者情况决定。1.根治性膀胱切除术的指征 根治性膀胱切除术的基本手术指征为T2-T4a, N0-X, M0浸润性膀胱癌,其他指征还包括高危非肌层浸润性膀胱癌T1G3肿瘤,BCG治疗无效的Tis,反复复发的非肌层浸润性膀胱癌,单靠TUR或腔内手术无法控制的广泛乳头状病变等;挽救性膀胱全切除术的指征包括非手术治疗无效、保留膀胱治疗后肿瘤复发和膀胱非尿路上皮癌。以上手术指征可独立选用,亦可综合应用。但应除外有严重合并症(心、肺、肝、脑、肾等疾病)不能耐受根治性膀胱切除术者。2.根治性膀胱切除术的相关事项 根治性膀胱切除术的手术范围包括:膀胱及周围脂肪组织、输尿管远端,并行盆腔淋巴结清扫术;男性应包括前列腺、精囊,女性应包括子宫、附件。近年来有研究对男性是否应将前列腺完整切除,女性是否应切除阴道及尿道提出疑问。如果手术尿道切缘阳性,原发肿瘤侵犯尿道、女性膀胱颈部或男性前列腺部,则需考虑施行全尿道切除。国内有学者认为若肿瘤累及前列腺、膀胱颈、三角区,或多发肿瘤、原位癌,应行全尿道切除术。亦有报道术中尿道远端切缘送快速病理检查,明确有无肿瘤累及,以决定是否需同时行尿道切除术。对于性功能正常的年龄较轻男性患者,保留性神经和精囊的手术可以使半数以上患者的性功能不受影响,但术后需严密随访,并且患者的长期转归有待进一步证实。目前根治性膀胱切除术的方式可以分为开放手术和腹腔镜手术两种。与开放手术相比,腹腔镜手术具有失血量少、术后疼痛较轻、恢复较快的特点,但手术时间并不明显优于开放性手术,而且腹腔镜手术对术者的操作技巧要求较高。近来机器人辅助的腹腔镜根治性膀胱切除术可以使手术更精确和迅速,并减少出血量。淋巴结清扫不仅是一种治疗手段,而且为预后判断提供重要的信息。目前主要有局部淋巴结清扫,常规淋巴结清扫和扩大淋巴结清扫三种。局部淋巴结清扫仅切除闭孔内淋巴结及脂肪组织;扩大淋巴结清扫的范围是:主动脉分叉和髂总血管(近端),股生殖神经(外侧),旋髂静脉和Cloquet淋巴结(远端),髂内血管(后侧),包括腹主动脉远端周围,下腔静脉周围,闭孔,两侧坐骨前和骶骨前淋巴结,清扫范围向上甚至可以扩展至肠系膜下动脉水平;常规淋巴结清扫的范围达髂总血管分叉水平,其余与扩大清扫范围相同;淋巴结清扫术应清除15个以上淋巴结。有学者认为扩大淋巴结清扫对患者有益,可以提高术后的5年生存率。阳性淋巴结占术中切除淋巴结的比例(淋巴结密度)可能是淋巴结阳性高危患者的重要预后指标之一。目前的随机对照研究显示,尽管术前放疗4-6周可以显著的降低浸润性膀胱癌的分期,但并不能显著延长患者的5年生存率。3.根治性膀胱切除术的生存率 随着手术技术和随访方式的改进,浸润性膀胱癌患者的生存率有了较大的提高。根治性膀胱切除术围手术期的死亡率为1.8%~3.0%,主要死亡原因有心血管并发症、败血症、肺栓塞、肝功能衰竭和大出血。患者的总体5年生存率为54.5%~68%,10年生存率为66%。若淋巴结阴性,T2期的5年和10年生存率分别为89%和78%,T3a期为87%和76%,T3b期为62%和61%,T4期为50%和45%。而淋巴结阳性患者的5年和10年生存率只有35%和34%。(二)保留膀胱治疗对于身体条件不能耐受根治性膀胱切除术,或不愿接受根治性膀胱切除术的浸润性膀胱癌患者,可以考虑行保留膀胱的综合治疗。鉴于浸润性膀胱癌较高的淋巴结转移比例,考虑施行保留膀胱治疗的患者需经过细致选择,对肿瘤性质、浸润深度进行综合评估,正确选择保留膀胱的手术方式,并辅以术后放射治疗和化学治疗,且术后需进行密切随访。浸润性膀胱癌保留膀胱的手术方式有两种:经尿道膀胱肿瘤切除术(TUR-BT)和膀胱部分切除术。对于多数保留膀胱的浸润性膀胱癌患者,可通过经尿道途径切除肿瘤。但对于部分患者应考虑行膀胱部分切除术:肿瘤位于膀胱憩室内、输尿管开口周围或肿瘤位于经尿道手术操作盲区的患者,有严重尿道狭窄和无法承受截石位的患者。近来有学者认为对于T2期患者,初次TUR-BT术后4~6周内再次行TUR-BT并结合化疗与放疗有助于保全膀胱。由于单一的治疗无法达到理想的保留膀胱的效果,所以目前保留膀胱的综合治疗多采取手术、化疗和放疗的三联综合治疗。该治疗方案的选择指征必须严格控制,且患者必须具有良好的依从性,才能得到较好的治疗效果。有研究显示,TURBT术后辅以顺铂类化疗方案及放射治疗,患者的治疗有效率可以达到60-80%。但是期间患者必须接受严密的观察,并及时的调整治疗方案。浸润性膀胱癌患者施行保留膀胱综合治疗的5年总体生存率为45%-73%,10年总体生存率为29%-49%。推荐意见:1.对于肌层浸润性膀胱尿路上皮癌首选根治性膀胱切除术,并同时进行淋巴结清扫。2.如肿瘤侵犯尿道、女性膀胱颈部或男性前列腺部,或手术尿道切缘阳性时,应行全尿道切除术。3.特殊情况下行保留膀胱的手术须经过仔细选择,应辅以放、化疗,并密切随访。七、尿流改道术尿流改道术尚无标准治疗方案。目前有多种方法可选,包括不可控尿流改道(noncontinent diversion)、可控尿流改道(continent diversion)、膀胱重建(bladder reconstruction)等。手术方式的选择需要根据患者的具体情况,如年龄、伴发病、预期寿命、盆腔手术及放疗史等,并结合患者的要求及术者经验认真选择。泌尿外科医生术前需与患者充分沟通,告知患者尿流改道的各种手术方式及其优缺点,取得一致意见后再决定尿流改道方式。保护肾功能、提高患者生活质量是治疗的最终目标。神经衰弱、精神病、预期寿命短、肝或肾功能受损、尿道或其它手术切缘阳性的患者对于复杂性尿流改道术属于禁忌证。(一)不可控尿流改道(noncontinent diversion)输尿管皮肤造口术(cutaneous ureterostomy)是一种简单、安全术式。由于输尿管直径小,输尿管皮肤吻合口狭窄发生率高。尿流改道相关的并发症输尿管皮肤造口术要明显低于回、结肠膀胱术。但是,皮肤造口处狭窄和泌尿道感染要高于回肠膀胱术。适用于预期寿命短、有远处转移、姑息性膀胱全切、肠道疾患无法利用肠管进行尿流改道或全身状态不能耐受手术者。回肠膀胱术(bricker operation)目前仍是一种经典的可选择的术式,主要缺点是需腹壁造口、终身佩戴集尿袋。早期并发症可达48%,包括尿道感染、肾盂肾炎、输尿管回肠吻合口漏或狭窄。长期随访结果表明,主要并发症是吻合口并发症(24%)和上尿路的功能和形态学上的改变(30%)。随着随访时间的增加,并发症相应增加,5年并发症为45%,15年并发症增加到94%,后组患者上尿路的改变和尿石形成分别达50%和38%。各种形式的肠道尿流改道中,回肠膀胱术的晚期并发症要少于可控贮尿囊或原位新膀胱。伴有短肠综合征、小肠炎性疾病、回肠受到广泛射线照射的患者不适于此术式。乙状结肠膀胱术(sigmoid bladder)对于有原发性肠道疾病或严重放射性盆腔炎和不愿意接受可控性膀胱术的患者,可作为回肠膀胱术的替代术式。横结肠膀胱术对于进行过盆腔放疗或输尿管短的患者可选用。(二)可控尿流改道(continent diversion)1.可控贮尿囊(continent reservior) 可控贮尿囊必须满足肠道去管重建成高容量低压贮尿囊,抗反流和控尿,能自行插管导尿的原则。随访发现该术式早,晚期并发症发生率分别为12%和37%。晚期并发症主要有输尿管狭窄或梗阻、尿失禁、导尿困难和尿路结石,代谢并发症也比较常见。在一项800多名患者的回顾性研究中表明,使用原位阑尾作输出道的回结肠贮尿囊的患者中有23.5%发生吻合口狭窄,使用回肠套叠乳头瓣作输出道的回结肠贮尿囊为15%。10%的患者有结石形成。可控贮尿囊适用于:①预期寿命较长、能耐受复杂手术;②双侧肾脏功能良好可保证电解质平衡及废物排泄;③无上尿路感染;④肠道未发现病变;⑤能自行导尿。2.利用肛门控制尿液术式 利用肛门括约肌控制尿液的术式包括:尿粪合流术,如输尿管乙状结肠吻合术,输尿管结肠、结肠直肠吻合术;尿粪分流术,如直肠膀胱术,直肠膀胱、结肠腹壁造口术。输尿管乙状结肠吻合术由于易出现逆行感染、高氯性酸中毒、肾功能受损和恶变等并发症,现已基本放弃,但这种术式的改良可以减少并发症的发生,所以还被一些治疗中心选择应用。主要用于预期寿命短、手术耐受性差的晚期癌症患者。采用肛门括约肌控制尿液的术式的患者肛门括约肌功能必须良好。患者在站立位不能容纳400~500ml的尿液1小时、神经源性膀胱为利用肛门控制尿液术式的禁忌证。(三)膀胱重建(bladder reconstruction)或原位新膀胱(orthotopic neobladder)近年来,原位新膀胱术逐渐已被各大医疗中心作为一些选择性病例根治性膀胱全切术后尿流改道的主要手术方式。可用于男性和女性患者。肠段的使用末端回肠应用较多,升结肠、盲肠、乙状结肠、胃应用相对较少。此术式主要优点是不需要腹壁造口,提高了生活质量和改变了自身形象。缺点是夜间尿失禁和排尿失败需要导尿或间歇性自我导尿。长期并发症包括昼夜尿失禁(分别为8%~10%,20%~30%)、输尿管肠道吻合口狭窄(3%~18%)、尿潴留(4%~12%)、代谢性疾病、维生素B12缺乏病等。另一缺点是尿道肿瘤复发,尿道肿瘤复发在男性、女性患者中约为1.5%~7%,如膀胱内存在多发原位癌或侵犯前列腺尿道则复发率高达35%。建议术前男性患者常规行前列腺尿道组织活检,女性行膀胱颈活检,或者术中行冷冻切片检查,术后应定期行尿道镜检和尿脱落细胞学检查。原位新膀胱术后生活质量是否好于非可控尿流改道还存在一定的争议。不同类型的原位新膀胱术与回肠膀胱术的总体并发症发生率一致,无明显差别。由于原位新膀胱术患者排尿需通过增加腹压完成,切口疝的发生率要比回肠膀胱高。在不同的新膀胱对比中,并发症发生率无显著差别。输尿管肠道吻合采用抗返流还是非抗返流仍存在着争论,抗返流吻合可保护肾功能,但易发生狭窄,应根据贮尿囊是否低压及术者经验予以选择。原位新膀胱的先决条件是完整无损的尿道和外括约肌功能良好,术中尿道切缘阴性。前列腺尿道有侵犯、膀胱多发原位癌、骨盆淋巴结转移、高剂量术前放疗、复杂的尿道狭窄以及不能忍受长期尿失禁的患者为原位新膀胱术的禁忌证。(四)腹腔镜手术腹腔镜或机器人辅助下腹腔镜手术已应用于多种尿流改道术,可作为一种选择,现多采用在腹腔镜下行膀胱切除术后通过小切口在腹腔外行尿流改道术。目前的技术条件下是否有必要完全在腹腔镜下完成尿流改道仍存在争议。腹腔镜下尿流改道方式选择原则与开放性手术基本相同。腹腔镜下膀胱全切-尿流改道术可在熟练掌握腹腔镜技术,掌握严格的适应证并且在患者的意愿下选择。推荐意见:1. 泌尿外科医生术前需与患者充分沟通,告知患者尿流改道的各种手术方式及其优缺点,取得一致意见后再决定尿流改道方式。应重视保护肾功能、提高患者生活质量。2. 原位新膀胱术可选择性地应用于没有任何禁忌证、肿瘤未侵犯尿道、术中尿道切缘阴性等选择性患者。3. 不可控尿流改道术可选择回肠膀胱术。八、膀胱癌的化疗与放疗(一)膀胱癌的化疗10%~15%的肌层浸润性膀胱癌患者在确诊时已出现转移,肌层浸润性膀胱癌行根治性膀胱切除术后,高达50%的患者会出现转移,5年生存率为36%~54%。对于T3~T4和(或)N+ M0膀胱癌高危患者,5年生存率仅为25%~35% 。膀胱癌对含顺铂的化疗方案比较敏感,总有效率为40%~75%,其中12%~20%的患者局部病灶获得完全缓解,约10%~20%的患者可获得长期生存。1.新辅助化疗 对于可手术的 T2~T4a期患者,术前可行新辅助化疗。新辅助化疗的主要目的是控制局部病变,使肿瘤降期,降低手术难度和消除微转移灶,提高术后远期生存率。新辅助化疗后,患者死亡率可下降12%~14%,5年生存率提高5%~7%,远处转移率降低5%,对于T3~T4a患者,其生存率提高可能更明显。新辅助化疗还被用做保留膀胱的手段,但这一方法备受争议。新辅助化疗的疗程尚无明确界定,但至少要用2~3个周期基于顺铂的联合化疗。2.辅助化疗 对于临床T2或T3期患者,根治性膀胱切除术后病理若显示淋巴结阳性或为pT3-4,术前未行新辅助化疗者术后可采用辅助化疗。膀胱部分切除患者术后病理若显示淋巴结阳性或切缘阳性或为pT3-4,术后亦可采用辅助化疗。辅助化疗可以推迟疾病进展,预防复发,但各项对于辅助化疗的研究由于样本量小、统计及方法学混乱,因此结果尚无定论[10]。3.对于临床T4a及T4b患者,若CT显示淋巴结阴性或发现不正常淋巴结经活检阴性,可行化疗或化疗+放疗,或手术±化疗(仅限于选择性cT4a患者)。CT显示有肿大淋巴结经活检阳性的,则行化疗或化疗+放疗[11]。4.转移性膀胱癌应常规行全身系统化疗,尤其是无法切除、弥漫性转移、可测量的转移病灶。身体状况不宜或不愿意接受根治性膀胱切除术者也可行全身系统化疗±放疗[12]。全身化疗2~3周期后进行评价,如肿瘤减小或稳定,则追加2周期化疗。如果化疗后肿瘤可手术切除,则术后继续2周期化疗,可延长患者生存期。如未行手术或放射治疗,则最多使用6周期化疗。如化疗2~3周期后评价肿瘤无反应,则应更换化疗方案[11]。已确立以下因素可影响预后:Karnofsky PS≤80%,以及内脏转移是独立的预后差的因素,这些叫“Bajorin”预后因素[13];其他如碱性磷酸酶或乳酸脱氢酶超过正常、病灶>3个、血红蛋白<10mg/dl等都提示预后差[14,15]。5.动脉导管化疗(intra-arterial chemotherapy) 通过对双侧髂内动脉灌注化疗药物达到对局部肿瘤病灶的治疗作用,对局部肿瘤效果较全身化疗好,常用于新辅助化疗[16-20]。文献报道,动脉导管化疗+全剂量放疗的完全缓解率可达78%~91%[16,17],动脉导管化疗作为辅助化疗效果不佳。化疗药物可选用MTX/CDDP或单用CDDP或5-Fu+ADM+CDDP+MMC等[16,21,22]。6.化疗方案(1)一线化疗方案:三种化疗药物活性较高,顺铂、吉西他滨、紫杉烷。2~3种化疗药物联合效果更好[11]。1) GC(吉西他滨和顺铂)方案:此联合化疗方案被认为是目前标准一线治疗方案,可被更多患者选用[23,24]。吉西他滨800~1000mg/m2第1、8、15天静脉滴注,顺铂70mg/m2第2天静脉滴注,每4周重复,共2~6个周期[11]。研究显示GC方案的CR为12%-22%【25,26】,PR为33%,中位疾病进展时间为23周,中位总生存时间为13.8个月,较MVAC方案耐受性好[25,26]。2) MVAC(氨甲蝶呤、长春碱、阿霉素、顺铂)方案:是传统上膀胱尿路上皮癌标准一线治疗方案[29]。氨甲蝶呤30mg/m2第1、15、22天静脉滴注,长春碱3mg/m2第2、15、22天静脉滴注,阿霉素30mg/m2第2天静脉滴注,顺铂70mg/m2第2天静脉滴注,每4周重复,共2~6个周期[11]。两项随机前瞻性研究已经证实MVAC方案效果明显好于单种药物化疗效果[30,31]。多项研究显示此方案的CR为12%-50%,有效率为50%~70%,中位总生存时间为14.8个月[25,26,28]。3)一线替代方案:如不能使用顺铂者,可使用含卡铂或紫杉烷类的化疗方案。但如肾功能正常,卡铂不能替代顺铂[11]。4) 如果联合放疗,则一线化疗可用顺铂单药、顺铂联合5-氟尿嘧啶或丝裂霉素-C联合5-氟尿嘧啶,这些药物可增加放疗的敏感性[2,11]。(2) 二线化疗方案:目前唯一被证实有效的二线化疗药物是长春氟宁。长春氟宁是一种新的第三代长春花碱药品,目标反应率为8.5%-18%,疾病控制率为67%,安全性好,并可延长患者生存【32,33】。其他单药可选用吉西他滨、培美曲塞、紫杉烷、异环磷酰胺等。联合用药可选用TC(紫杉醇和顺铂)方案[34,35],GD(吉西他滨和多西他赛)方案[36],TCa(紫杉醇和卡铂)方案[37],DC(多西他赛和顺铂)3周方案[38],GT(吉西他滨和紫杉醇)方案[39-41],以及CMV(氨甲蝶呤联合长春碱和顺铂)方案,CAP(环磷酰胺联合阿霉素和顺铂)方案[42],GCT(吉西他滨联合顺铂和紫杉醇)方案[43],GCaT(吉西他滨联合卡铂和紫杉醇)方案[44],CGD(顺铂联合吉西他滨和多西他赛)方案,ICP(异环磷酰胺联合顺铂和紫杉醇)方案,等[2,11]。(二)膀胱癌的放疗肌层浸润性膀胱癌患者在某些情况下,为了保留膀胱不愿意接受根治性膀胱切除术,或患者全身条件不能耐受根治性膀胱切除手术,或根治性手术已不能彻底切除肿瘤以及肿瘤已不能切除时,可选用膀胱放射治疗或化疗+放射治疗[2]。但对于肌层浸润性膀胱癌,单纯放疗患者的总生存期短于根治性膀胱切除术 [41]。1.根治性放疗 膀胱外照射方法包括常规外照射、三维适形放疗及调强适形放疗。单纯放射治疗靶区剂量通常为60~66Gy,每天剂量通常为1.8~2Gy,整个疗程不超过6~7周[46,47]。目前常用的放疗日程为:①50~55Gy,分25~28次完成(> 4周);②64~66Gy,分32~33次完成(> 6.5周)[48]。放疗的局部控制率约为30%~50%[49],肌层浸润性膀胱癌患者5年总的生存率约为40%~60%,肿瘤特异生存率为35%~40%,局部复发率约为30%[50]。欧洲文献报道,T1/ T2期小肿瘤患者可通过膀胱切开(行或未行膀胱部分切除)显露肿瘤后置入放射性碘、铱、钽或铯行组织内近距离照射,再联合外照射和保留膀胱的手术,从而达到治疗目的。根据肿瘤分期不同,5年生存率可达60%~80%[51]。2.辅助性放疗 通过术前4-6周的放疗,可使40-65%的患者肿瘤降期,使10-42%的患者提高局部肿瘤控制率,但根治性膀胱切除术前放疗对延长患者生存是否有益尚不明确[52-55],因此不推荐术前放疗。膀胱全切或膀胱部分切除手术未切净的残存肿瘤或术后病理切缘阳性者,可行术后辅助放疗[56]。3.姑息性放疗 通过短程放疗(7 Gy×3天;3~3.5 Gy×10天)可减轻因膀胱肿瘤巨大造成无法控制的症状,如血尿、尿急、疼痛等。但这种治疗可增加急性肠道并发症的危险,包括腹泻和腹部痉挛疼痛[48,57]。(三)保留膀胱的治疗策略主要针对T2和T3a的尿路上皮癌患者。方法包括单纯经尿道电切手术、经尿道电切手术联合化疗、经尿道电切手术联合放疗、联合放化疗。(1)单纯经尿道电切手术 仅对少部分肿瘤局限于浅肌层、且对肿瘤基底再次分期活检阴性的患者可采用,或对于不适合做全膀胱切除手术或拒绝做全膀胱切除手术的患者也可采用[58]。但基底活检为pT0或pT1的患者中有一半会进展成浸润性膀胱癌而被迫行全膀胱切除,肿瘤特异死亡率占47%[58]。(2)经尿道电切手术联合外放射治疗 主要针对不适合膀胱癌根治术或不能耐受化疗的患者。这组患者5年存活率从30%到60%,肿瘤特异存活率从20%到50%[47,59-62]。(3)经尿道电切手术联合化疗 病理完全反应率可为8-26%[63-65],对T3/T4使用顺铂为基础的化疗,其CR和PR分别为11%和34%[66,67]。3周期化疗后,通过膀胱镜和活检再次评估,如无残余病灶,则也要警惕有残余病灶存在的可能;如病灶仍存在,则行挽救性全膀胱切除[11]。(4)经尿道电切手术联合放、化疗 最大限度经尿道电切手术后,以顺铂为基础的化疗联合放疗可使完全缓解率达到60%-80%,可使40%-45%的患者保留完整膀胱存活4-5年,长期存活达50%-60%(与全膀胱切除相媲美)。如果联合治疗不敏感,则推荐早期行全膀胱切除[50,68,69]。(5)化疗联合膀胱部分切除术 不到5%的肌层浸润型膀胱癌可通过膀胱部分切除达到治愈的目的。可使约27%的患者避免全膀胱切除手术[70]。推荐意见:1.化疗和放疗主要作为膀胱癌的辅助性治疗。2.全身化疗是转移性膀胱癌的标准治疗。3. 肌肉浸润性膀胱癌根治术前可选择新辅助化疗。4. 肌肉浸润性膀胱癌根治术前不建议进行新辅助放疗5.化疗应选择含铂类的联合化疗方案,GC方案和MVAC方案为一线化疗方案。6.化疗或放疗可作为根治性手术的选择性替代方式,但疗效次于根治性手术。7.对需要保留膀胱的患者,可行经尿道切除膀胱肿瘤联合放化疗,但应密切随访。九、膀胱癌患者的生活质量、预后与随访(一)生活质量健康相关生活质量(health-related quality of life, HRQL)研究目前已被广泛应用于肿瘤和慢性病临床治疗方法的筛选、预防性干预措施效果的评价以及卫生资源分配的决策等方面。但是在国内,对于膀胱癌患者生活质量的研究尚未引起泌尿外科医师的足够重视。膀胱癌患者生活质量评估应包含身体、情绪、社会活动方面的内容以及相关的并发症(如排尿问题、尿瘘、皮肤问题、性功能问题等)。生活质量评估主要是通过适宜的量表来完成。目前膀胱癌研究中应用较多的生活质量评估量表包括FACT ( functional assessment of cancer therapy )-G[1],EORTC QLQ-C30[2]和SF (short form)-36[3]。非肌层浸润性膀胱癌患者生活质量的相关研究较少,并且主要集中于术后灌注BCG的患者。随访中发现,非肌层浸润性膀胱癌患者的总体健康严重受损。患者接受第一次TUR-BT时心理健康受损最严重,而躯体功能、躯体角色、情感角色和社会功能在第二次或第三次TUR-BT时受损最严重。如果患者接受第四次或更多次TUR-BT,则除了总体健康外,其他几方面都将回到正常水平。此外,排尿问题(如血尿和尿频、尿急、尿痛等)是术后治疗过程中最为常见的症状,严重影响患者的生活质量,尤其是在治疗早期,但随着治疗的持续尤其是当治疗间期延长后将逐步减轻[4,5]。肌层浸润性膀胱癌患者生活质量研究的焦点是全膀胱切除术后接受不同尿流改道术式者相互之间的比较以及与正常人群之间的比较。总体来讲,接受可控尿流改道或原位新膀胱手术患者的生活质量优于接受非可控性尿流改道手术的患者[6-11],但是也有文献报道指出前者并不优于后者[12-14]。对于接受保留膀胱手术、放疗和/或化疗治疗的肌层浸润性膀胱癌患者,虽然少有文献对其生活质量进行研究,但是膀胱相关并发症的发生率相对较低[15-17]。对患者术后生活质量进行评估时应充分考虑患病时间、患者年龄、性格、相处能力、文化背景、对手术方案及其术后可能面临处境的了解以及患者完成问卷的方式、地点等各种因素的影响。推荐意见:1.泌尿外科医师应该充分重视膀胱癌患者治疗后的健康相关生活质量。2.治疗前,泌尿外科医师应该与膀胱癌患者就治疗方法选择及其并发症进行充分讨论,以使患者治疗后获得最佳的生活质量。(二)膀胱癌的预后因素膀胱癌的预后与肿瘤分级、分期、肿瘤大小、肿瘤复发时间和频率、肿瘤数目以及是否存在原位癌等因素密切相关,其中肿瘤的病理分级和分期是影响预后的最重要因素[18-21]。国内一项研究显示,各期膀胱癌患者5年生存率分别为Ta~T1期91.9%、 T2期84.3%、T3期43.9%、T4期10.2%。各分级膀胱癌患者5年生存率分别为G1级91.4%、 G2级82.7%、 G3级62.6%[22]。对于非肌层浸润性膀胱癌,可以通过EORTC(European Organization for Research and Treatment of Cancer)制定的一个综合肿瘤数目、大小、复发频率、分级、分期和有无伴发原位癌等6项指标的评分系统来评估TUR-BT术后近期和远期复发及进展的概率(表3~表5),并根据复发的危险性和进展的危险性分别相应的将患者分为低危、中危和高危[23]。近年来随着对肿瘤分子机制认识的加深,许多肿瘤标记物相继被发现可用于膀胱癌的预后判断。研究发现,核基质蛋白22 (NMP-22)、端粒酶(telomerase)、血管内皮生长因子 (vascular endothelial growth factor, VEGF)、透明质酸酶 (hyaluronidase, HAase)、增殖相关核抗原Ki-67以及p53基因等均对膀胱癌的预后判断有一定价值[24-28]。但必须指出的是,目前膀胱癌肿瘤标记物的研究尚处于实验室阶段,临床上尚没有一种标记物能准确估计膀胱癌的预后。(三)膀胱癌患者的随访膀胱癌患者治疗后随访的目的是尽早发现局部复发和远处转移,如果有适应证且有可能,应及早开始补救治疗。膀胱癌患者的随访方案目前无前瞻性对照研究证据支持,应该根据预后评估和所采取的治疗方式(如TUR-BT、膀胱切除术、尿流改道方式等)来制定。1.非肌层浸润性膀胱癌的随访 在非肌层浸润性膀胱癌的随访中,膀胱镜检查目前仍然是金标准,泌尿外科医师应该尽可能地帮助患者克服恐惧心理而接受膀胱镜检查。同时一旦发现异常则应该行病理活检。B超、尿脱落细胞学以及IVU等检查在非肌层浸润性膀胱癌的随访中亦有一定价值,但均不能完全代替膀胱镜检的地位和作用[29-33]。所有的非肌层浸润性膀胱癌患者都应该在术后3个月接受第一次膀胱镜检查,但是如果手术切除不完整、创伤部位有种植或者肿瘤发展迅速则需要适当提前[34]。以后的随访应根据肿瘤的复发与进展的危险程度决定。一旦患者出现复发,则治疗后的随访方案须重新开始。推荐意见:1.所有患者应以膀胱镜为主要随访手段,在术后3个月接受第一次复查。2.低危肿瘤患者如果第一次膀胱镜检阴性,则9个月后进行第二次随访,此后改为每年一次直至5年。3.高危肿瘤患者前2年中每3个月随访一次,第三年开始每6个月随访一次,第五年开始每年随访一次直至终身。4.中危肿瘤患者的随访方案介于两者之间,由个体的预后因素决定。2.根治性膀胱切除术后的随访 膀胱癌患者接受根治性膀胱切除术和尿流改道术后必须进行长期随访,随访重点包括肿瘤复发和与尿流改道相关的并发症。根治性膀胱切除术后肿瘤复发和进展的危险主要与组织病理学分期相关,局部复发和进展以及远处转移在手术后的前24个月内最高,24~36个月时逐渐降低,36个月后则相对较低[35]。肿瘤复发通过定期的影像学检查很容易发现,但是间隔多长时间进行检查仍然存在着争论。有学者推荐pT1期肿瘤患者每年进行一次体格检查、血液生化检查、胸部X线片检查和B超检查(包括肝、肾、腹膜后等);pT2期肿瘤患者6个月进行一次上述检查而pT3期肿瘤患者每3个月进行一次。此外,对于pT3期肿瘤患者应该每半年进行一次盆腔CT检查[36]。需要特别指出的是,上尿路影像学检查对于排除输尿管狭窄和上尿路肿瘤的存在是有价值的,上尿路肿瘤虽然并不常见,但是一旦发现往往需要手术治疗[37]。根治性膀胱切除术后尿流改道患者的随访主要包括手术相关并发症(如反流和狭窄)、替代物相关代谢问题(如维生素B12缺乏所致贫血和外周神经病变)、尿液贮存相关代谢问题(水电解质紊乱)、泌尿道感染以及继发性肿瘤问题(如上尿路和肠道)等方面。推荐意见:1.根治性膀胱切除术后患者应该进行终身随访。2.随访间隔:pT1期每年一次,pT2期每6个月一次,pT3期每3个月一次。3.随访内容应包括体格检查、血液生化检查、胸部X线片检查和B超检查(包括肝、肾、腹膜后等)。对于pT3期肿瘤患者可选择每半年进行一次盆腔CT检查。可选择上尿路影像学检查以排除输尿管狭窄和上尿路肿瘤的存在。4.尿流改道术后患者的随访主要围绕手术相关并发症、代谢并发症、泌尿道感染以及继发性肿瘤等几方面进行。十、膀胱非尿路上皮癌(一)鳞状细胞癌 (Squamous cell carcinoma, SCC)膀胱鳞状细胞癌(SCC)可分为非血吸虫病性膀胱SCC和血吸虫病性膀胱SCC。诊断主要靠膀胱镜活检。单纯的膀胱SCC患者应选择根治性膀胱切除术,高分级、高分期肿瘤术前放疗有助于预防盆腔复发,在无有效化疗药物的情况下可选择根治性手术之前放疗[1,2]。膀胱SCC的5年生存率约为50%[1,2]。血吸虫病性膀胱SCC的预后相对较好[1]。1.非血吸虫病性膀胱鳞状细胞癌 细菌感染、异物、慢性下尿路梗阻或膀胱结石等引起的慢性炎症,以及膀胱粘膜白斑、长期留置导尿管等可能与膀胱SCC的发生有关[3-5]。非血吸虫病性膀胱SCC好发于膀胱三角区和侧壁,主要是溃疡和浸润,很少呈乳头样生长,可伴有膀胱憩室或膀胱结石。约8%膀胱SCC发生转移[2]。血尿是主要的临床表现,93%的患者伴有泌尿系统感染[6]。本病单纯放疗效果差[7],根治性膀胱切除术疗效优于放疗[8],术前放疗加根治性膀胱切除术比单纯根治性膀胱切除术效果更好[2]。膀胱SCC是一种化疗抵抗的肿瘤,目前还未发现有效的化疗方案[9]。2.血吸虫病性膀胱鳞状细胞癌 血吸虫病性膀胱SCC的发生可能与血吸虫存在导致的细菌和病毒感染有关,而非寄生虫本身[10]。维生素A缺乏也可能是膀胱上皮鳞状化生及肿瘤发生的重要原因之一。血吸虫病性膀胱SCC的平均发病年龄比非血吸虫病性膀胱SCC低10~20岁。主要症状是尿频、尿痛和血尿。肿瘤多发于膀胱后壁的上半部分或顶部,很少发生于三角区。确诊主要依靠膀胱镜检查活检以及麻醉状态下仔细的双合诊[11]。根治性膀胱切除术是血吸虫病性膀胱SCC治疗的主要方法。研究显示术前放疗可改善高分级、高分期肿瘤患者的预后[12]。(二)腺癌 (Adenocarcinoma)根据组织来源膀胱腺癌可分为三种类型:原发性非脐尿管腺癌、脐尿管腺癌、转移性腺癌。诊断主要依靠膀胱镜活检,B超、CT以及MRI等检查可显示肿瘤大小、侵犯范围及临床分期,特别是对脐尿管腺癌,当肿瘤未侵及膀胱粘膜时,膀胱镜检可无异常发现。1.非脐尿管腺癌 非脐尿管腺癌可能因移行上皮腺性化生引起[13]。长期的慢性刺激、梗阻及膀胱外翻则是引起化生的常见原因[14,15]。血吸虫感染也是腺癌发生原因之一,在血吸虫流行地区膀胱腺癌约占膀胱癌的10%[16]。膀胱腺癌主要症状有血尿、尿痛、膀胱刺激症状、黏液尿。原发性膀胱腺癌发生于膀胱三角区及膀胱侧壁,病变进展较快,多为肌层浸润性膀胱癌[16]。非脐尿管腺癌的患者伴腺性膀胱炎比原位癌更常见[17]。临床就诊时大多数已属局部晚期,宜行根治性膀胱切除术以提高疗效。经尿道切除或膀胱部分切除术的疗效差[18-20]。术后辅以放射治疗,可以提高肿瘤无复发生存率[21]。对于进展期和已有转移的腺癌可以考虑化疗,一般采用5-氟尿嘧啶为基础的化疗,M-VAC方案化疗无效[22]。2.脐尿管腺癌 脐尿管腺癌可能与脐尿管上皮增生及其内覆移行上皮腺性化生有关[23,24],约占膀胱腺癌的1/3[25]。脐尿管腺癌只发生在膀胱顶部前壁,膀胱粘膜无腺性膀胱炎和囊性膀胱炎及肠上皮化生,肿瘤集中于膀胱壁,即肌间或更深层,而非粘膜层,可见脐尿管残留[26]。脐尿管腺癌可浸润到膀胱壁深层、脐、Retzius间隙及前腹壁。脐尿管腺癌的治疗主要为手术治疗, 包括扩大性膀胱部分切除术和根治性膀胱切除术。放疗和化疗的效果不佳[27]。近年来脐尿管腺癌采用扩大性膀胱部分切除术受到重视[28],手术应尽可能的整块切除膀胱顶、脐尿管和脐,切除范围包括部分腹直肌、腹直肌后鞘、腹膜及弓状线。术后复发和转移是治疗失败的主要原因,一般在术后2年内发生[29]。常见的转移部位是骨、肺、肝和盆腔淋巴结[28]。脐尿管腺癌诊断时往往分期较高,有较高的远处转移风险。美国M.D. Anderson肿瘤中心的经验:边缘阴性与否和淋巴结情况是影响预后的重要因素,总体5年生存率为40%,平均生存46个月[30]。3.转移性腺癌 转移性腺癌是最常见的膀胱腺癌,原发病灶包括来自直肠、胃、子宫内膜、乳腺、前列腺和卵巢。治疗上以处理原发病为主的综合治疗。(三)未分化癌(小细胞癌 Small cell carcinoma)未分化癌少见,已报道有一种小细胞癌类型,组织学上类似肺小细胞癌。肿瘤好发于膀胱两侧壁和膀胱底部。膀胱小细胞癌瘤体直径往往较大,平均约5cm[31]。与尿路上皮癌相似,膀胱小细胞癌主要通过淋巴转移,不同点在于其更具侵袭性,转移的更早、更快。最常见的转移部位依次为淋巴结、肝脏、骨骼、肺和大脑[32]。就诊时患者往往已有深肌层浸润[33]。膀胱小细胞癌的诊断同尿路上皮癌,但应考虑有无远处转移。膀胱小细胞癌与膀胱尿路上皮癌在CT上的区别是:膀胱小细胞癌广基、无蒂、息肉样改变,向膀胱壁内浸润明显,在未出现膀胱邻近器官或淋巴结转移时往往已侵犯膀胱全层[34]。膀胱小细胞癌细胞病理学特征为零散的、相互孤立、圆形、大小均匀的小细胞,细胞学上相邻的肿瘤细胞缺乏巢状或腺状结构是膀胱小细胞癌最重要的特征[33]。小细胞癌可分为局限期和广泛期,局限期是指任何分期、最大区域淋巴结转移不超过2cm、无远处转移,其余均属广泛期[35]。局限期治疗考虑采用小细胞肺癌的化疗方案做辅助化疗或者新辅助化疗,并联合局部治疗(手术或放疗)[9,35]。研究认为新辅助化疗有助于提高生存率[36]。手术治疗应选择根治性膀胱切除术,病理分期为T3、T4期考虑术后辅助化疗,化疗一般选用顺铂和依托泊甙[31]。广泛期主要采用放疗或/和化疗为主的综合治疗[35]。(四)混合细胞癌混合细胞癌是指原发于膀胱的两种不同类型恶性肿瘤同时出现或并存。通常以鳞癌、腺癌或小细胞癌与尿路上皮癌共生。其病程进展快,恶性程度高,预后极差,治疗上建议行根治性膀胱切除术[37]。根治术后没有证据表明辅助化疗有效(小细胞癌除外)。如果含有小细胞癌的成分,根治性膀胱切除术后根据分期选择小细胞癌的辅助化疗方案[38]。推荐意见:1.膀胱非尿路上皮癌的治疗原则是选择根治性膀胱切除术。2.高分级、高分期的膀胱鳞状细胞癌术前放疗可改善预后。3.膀胱脐尿管腺癌可选择扩大性膀胱部分切除术,非脐尿管腺癌根治性膀胱切除术后可选择辅助放疗或/和化疗。4.病理分期为T3、T4期膀胱小细胞癌可选择新辅助化疗和术后辅助化疗。推荐意见:1.膀胱非尿路上皮癌的治疗原则是选择根治性膀胱切除术。2.高分级、高分期的膀胱鳞状细胞癌术前放疗可改善预后。3.膀胱脐尿管腺癌可选择扩大性膀胱部分切除术,非脐尿管腺癌根治性膀胱切除术后可选择辅助放疗或/和化疗。4.病理分期为T3、T4期膀胱小细胞癌可选择术后辅助化疗。
马洪贵 副主任医师 贵州医科大学附属医院 泌尿外科8004人已读 - 精选 前列腺癌的早期诊断和治疗
前列腺癌病灶MRI,T2WI(T2加权成像)表现为低信号,ADC(表观弥散系数)降低,DWI(弥散加权成像)呈现高信号。虽然有些患者MRI和骨扫描,PSA15.57ng/ml都间接提示前列腺癌,然而只有病理穿刺的结果才是一锤定音的最终结论。有些非特异性肉芽肿性前列腺炎临床表现容易和前列腺癌的MRI、PSA变化类似,只有依赖病理穿刺活检来鉴别,而且对日后逐步进展的前列腺癌变更治疗方案提供依据。尽管切缘阳性与术后生化复发密切相关,但是否它一定预示临床进展及更高的前列腺癌特异死亡率仍受到质疑。切缘阳性患者建议采取术后辅助性放疗,放疗对术后尿控功能有一定影响,可以等尿控功能恢复后再进行放疗。而对于那些术前低危,担心放疗副作用的患者,也可以采取密切监测,待PSA上升至一定值时采取挽救性放疗。此外,除了放疗,还可以联合辅助内分泌治疗,可能较单纯放疗使患者进一步获益。多参数磁共振成像mpMRI在前列腺癌的诊断中具有很好的诊断效能。基于多参数核磁共振的前列腺影像报告和数据评分系统(ProstateImagingReportingandDataSystem,PI-RADS),适用于前列腺癌的定位、诊断和危险分组,主要是根据前列腺T2加权显像(T2WI)、弥散加权成像(DWI)及动态对比增强(DCE)的mpMRl综合表现,对出现具有临床意义前列腺癌的可能性给岀了评分方法。PI-RADS评分与前列腺癌的相关性评分前列腺癌发生概率前列腺穿刺阳性率1非常低(极不可能出现)-2低(不太可能出现)-3中等(可疑存在)20%4高(可能存在)50%5非常高(极有可能出现)80%PI-RADS:1-2分不建议进行临床干预,但必须考虑局部情况、实验室检查、临床病史等其他因素PI-RADS:3分是否进行前列腺穿刺取决于多参数核磁共振之外的因素PI-RADS:4-5分应考虑进行靶向和系统性活检有时PSA值不是太高并不代表前列腺癌的进展程度
丁翔 主任医师 苏州大学附属第一医院 泌尿外科3382人已读 - 精选 前列腺癌的TNM分期、分级和危险因素
1、前列腺癌的TNM分期目前,前列腺癌的分期标准最常采用的是2002年AJCC的TNM分期系统2、前列腺癌的病理分级在前列腺癌的病理分级方面,目前最常使用Gleason评分系统。前列腺癌组织被分为主要分级区和次要分级区,每区的Gleason分值在1-5,Gleason评分是把主要分级区和次要分级区的Gleason分值相加,形成癌组织分级常数。分级标准:Gleason 1:癌肿极为罕见。其边界很清楚,膨胀型生长,几乎不侵犯基质,癌腺泡很简单,多为圆形,中度大小,紧密排列在一起,其胞浆和良性上皮细胞胞浆极为相近。Gleason 2:癌肿很少见,多发生在前列腺移行区,癌肿边界不很清楚,癌腺泡被基质分开,呈简单圆形,大小可不同,可不规则,疏松排列在一起。Gleason 3:癌肿最常见,多发生在前列腺外周区,最重要的特征是侵润性生长,癌腺泡大小不一,形状各异,核仁大而红,胞浆多呈碱性染色。Gleason 4:癌肿分化差,浸润性生长,癌腺泡不规则融合在一起,形成微小乳头状或筛状,核仁大而红,胞浆可为碱性或灰色反应。Gleason 5:癌肿分化极差,边界可为规则圆形或不规则状,伴有浸润性生长,生长型式为片状单一细胞型或者是粉刺状癌型,伴有坏死,癌细胞核大,核仁大而红,胞浆染色可有变化。3、前列腺癌的危险因素分析D’Amico等提出的风险评估标准是目前临床上最常用的前列腺癌危险因素分类方法,它根据患者血清PSA、Gleason评分和临床分期将前列腺癌分为低、中、高危三类,可以用于指导治疗和判断预后。
朱寅杰 副主任医师 上海交通大学医学院附属仁济医院(东院) 泌尿外科7.6万人已读 - 精选 腺性膀胱炎216例治疗方案选择
【摘要】 目的 探讨腺性膀胱炎的治疗方案。方法 对216 例经膀胱镜及病理学检查确诊的腺性膀胱炎,按类型不同分为A组(慢性炎症型及黏膜无显著改变型)40例及B组(乳头状型及滤泡样或绒毛膜样水肿型)176例,分别予保守治疗及经尿道电切并术后即刻吡柔比星膀胱灌注。结果 随访209例,随访6~72个月,中位随访时间28个月。A组28例治愈,6例好转,6例无效改电切及吡柔比星膀胱灌注,仅1例有效。B组治愈91例,好转37例,无效28例,复发13例,其中1例3年内复发4次,行膀胱部分切除后治愈,无一例发生恶变。结论 早期腺性膀胱炎保守治疗疗效满意,而乳头状型、滤泡样或绒毛膜样水肿型腺性膀胱炎以及广泛肠上皮化生型宜采用经尿道电切,术后可予单剂吡柔比星即刻膀胱灌注化疗,无须维持膀胱灌注化疗。【关键词】 膀胱炎;治疗学;膀胱灌注【中图分类号】R694.3 【文献标志】ATreatment of Glandulars Cystitis(Reports of 216 cases) LU Jia-sun,WEN Ji-ling, QIU Guang-min, WEN Xiao-fei, YANG Bo, CHEN Xing-yiDept. of Urology, East Hospital of Tongji University, Shanghai 200120,China.【Abstract】 Objective To approach the treatment of cystitis glandularis. Methods Two hundred and sixteen cases of cystitis glandularis were diagnosed by cystoscopy and pathological examination and divided into Group A(chronic inflammation pattern and no-significant-change in the mucosa pattern) and Group B(papilloma-like pattern and follicle or chorion-like oedema pattern).Group A were treated by antibiotic while Group were treated by transurethral resection and bladder instillation of pirarubicin postoperation immediately. Results Follow-up for 209 patients ranged from 6 months to 72 months (median 28 months). In group A,28 cases were fully cured, 6 cases were improved and 6 cases were ineffective which were subsequent treated by transurethral resection and bladder instillation,only one case was improved. In group B,91 cases were cured, 37 cases were improved,28 cases were ineffective and 13 cases recurred. One case recurred four times in three years, and cured after treated with by partial cystectomy. There is no any cases developed canceration. Conclusion Cystitis glandularis of initial stage was effective by anti-infective therapy. And transurethral plasmakinetic resection is effective for the treatment of other cystitis glandularis(papilloma-like pattern,follicle or chorion-like oedema pattern and extensive intestinal metaplasia pattern).Bladder instillation of pirarubicin postoperation immediately is enough.【Key words】 Cystitis; Therapeutics; Irrigation of bladder腺性膀胱炎(glandular cystisis, GC)是一种膀胱黏膜上皮反应性增生改变,1887年由Von Limberk首先报道。近年来发病率有所增加,但目前尚无标准治疗方案。我院自 2002年6月至 2008年6月,根据腺性膀胱炎不同类型,分别采用保守治疗、经尿道电切并术后即刻吡柔比星膀胱灌注治疗216例,效果满意,现报道如下。1 资料与方法1.1 一般资料经膀胱镜及病理学检查确诊的腺性膀胱炎216 例,男性46例,女性170例,平均年龄43.2(21~75)岁。病程3个月至3年。临床表现为尿频、尿急、尿痛等尿路刺激症状115例(53%) ,下腹及会阴痛41例(19%),镜下血尿82例(38%),伴焦虑、紧张、失眠等精神症状21例(10%)。其中膀胱颈部抬高致膀胱出口梗阻34例(16%),尿道狭窄22例(10%),合并前列腺增生17例(8%),肾轻度积水6例(3%)。其中65例患者初诊为尿路感染,抗感染治疗后尿中白细胞消失,但镜下血尿及尿频仍持续存在,后经膀胱镜检及活检确诊为腺性膀胱炎。216例均行超声检查,发现膀胱内占位性病变22例。根据膀胱镜检查,将腺性膀胱炎分为四种类型:乳头状型62例(29%),滤泡样或绒毛膜样水肿型114例(53%),慢性炎症型23例(11%),黏膜无显著改变型17例(8%)。病变位于膀胱颈部31例(14%)、三角区117例(54%)、三角区及颈部34例(16%)、输尿管口周围12例(6%),呈弥漫性5例(2%)。全部患者均经膀胱镜活检病理检查证实为腺性膀胱炎。1.2 治疗方法根据腺性膀胱炎类型,将患者分为2组。A组:慢性炎症型及黏膜无显著改变型;B组:乳头状型及滤泡样或绒毛膜样水肿型。A组在排除梗阻及结石因素后,采用保守治疗,予口服左氧氟沙星抗感染治疗,0.2g/次,每天2次,疗程2~3周。3月后如症状无改善或膀胱镜下病变仍然存在,则予经尿道电切及吡柔比星灌注。B组采用经尿道电切及术后即刻吡柔比星膀胱灌注治疗。采用英国Gyrus公司等离子体切割系统或德国STORZ电切镜,腰麻或持续硬膜外麻醉下经尿道行膀胱病损粘膜电切术,电切范围为超过肉眼可见病变周边1cm。电切深度至浅肌层,病变范围位于输尿管口者先留置输尿管导管后电切,切除后用Ellick冲洗器将组织吸出送病理检查,尿道狭窄者予尿道扩张,膀胱颈部抬高者行膀胱颈部电切术。术后留置导尿管,并即刻予吡柔比星30 mg加注射用水30 ml膀胱灌注,保留30 min,术后第2天拔除导尿管后出院。术后不再定期予药物膀胱灌注。1.3 疗效判断标准因术后3个月内手术创面未完全修复,3月后复诊判断疗效。治愈:症状完全消失,膀胱镜复查加活检黏膜正常。好转:症状减轻,膀胱镜检黏膜无明显异常,但活检有慢性炎症表现者。治愈和好转均视为有效。无效:症状无改善甚至加剧者,术后膀胱镜及活检发现仍有腺性膀胱炎病变。复发:术后3个月镜检加活检无异常,但6个月后复查出现腺性膀胱炎者。2 结 果209例获得随访,因联系方式更改失访7例,随访6~72个月,中位随访时间28个月。A组40例,均获随访,保守治疗治愈28例,好转7例,6例无效改经尿道电切及术后即刻吡柔比星膀胱灌注治疗,仅1例好转。B组176例,169例获得随访,治愈91例,好转37例,无效28例,复发13例,其中12例经再次电切及吡柔比星膀胱灌注后治愈或好转,1例3年内复发4次,行膀胱部分切除后治愈,无一例发生恶变。3 讨 论腺性膀胱炎的发病率约占膀胱疾病的1%。近年来由于腔内泌尿外科技术的发展和普及,临床和病理医师对本病认识的提高,其患病率有增加的趋势【1】。腺性膀胱炎主要表现为尿频、尿痛、下腹及会阴痛和镜下血尿,部分患者有肉眼血尿。Kaya C【2】曾报道膀胱三角区一巨大的腺性膀胱炎导致严重的梗阻症状。诊断主要靠膀胱镜检和病理活检。与尿路上皮肿瘤常规行尿细胞学检查不同,腺性膀胱炎患者通过尿细胞学检查发现腺细胞很罕见【3】。但至今对腺性膀胱炎的病因及生物学意义尚未完全明了,多数腺性膀胱炎是一种继发性病理改变,慢性感染、下尿路梗阻等可能诱发腺性膀胱炎并促进其发展。陈志强等【4】提出腺性膀胱炎可分为早期和后期,早期包括慢性炎症型和黏膜无显著改变型,发病率高,不应视为癌前病变。但若慢性刺激因素持续存在,则可发展为后期腺性膀胱炎,包括广泛肠上皮化生型、乳头状瘤样型和肠腺瘤型。后期腺性膀胱炎存在较短时间内恶变可能,应视作癌前病变,积极进行外科治疗。早期腺性膀胱炎单纯行局部电切不仅不能改善症状,部分患者症状反而加重,病变复发率高。庄乾元等【5】对于早期轻症患者采取保守治疗,其疗效与手术疗效无明显差异。保守治疗后,膀胱内病变甚至可向好的方向发展,滤泡样结构消失。本组资料也表明,慢性炎症型和黏膜无显著改变型患者保守治疗有效率较高,而保守治疗无效者即便行手术治疗,疗效亦不佳。目前腺性膀胱炎多采用经尿道电切治疗,也有采用钬激光治疗的报道【6】。电切术后多按照浅表性膀胱移行上皮癌行膀胱灌注化疗。但是,膀胱化疗药物的灌注,患者术后膀胱刺激症状改善不明显,部分患者症状并无好转,并且加重了患者的经济负担,耗费了较多的医疗资源。腺性膀胱炎有恶变可能,但恶变率很低。国内外多数报道为腺性膀胱炎并发膀胱肿瘤【7】。我们认为,腺性膀胱炎病理改变在于膀胱黏膜层,可按低危非肌层浸润膀胱尿路上皮癌化疗方案【8】,术后予单剂吡柔比星即刻膀胱灌注化疗即可,而无须维持膀胱灌注化疗。如合并膀胱肿瘤,则按照膀胱肿瘤治疗。我们的长期随访结果证实,术后予单剂化疗药物即刻膀胱灌注效果良好,随访至今无1例发生恶变。对病变范围广泛、高度不典型增生者,如高度怀疑或已有癌变,可考虑作全膀胱切除术。Black【9】及Coelho RF【10】对症状较重及反复复发的患者,特别是双侧输尿管梗阻的,采用了全膀胱前列腺切除加回肠新膀胱术治疗。但此类手术治疗适应证应从严掌握。腺性膀胱炎临床进程尚不清楚,需要长期随访。我们建议患者术后定期复查尿常规,了解有无慢性尿路感染存在,术后定期复查膀胱镜,了解有无复发、恶变及膀胱黏膜愈合情况。【参考文献】[1]. 高新.经尿道腺性膀胱炎电切术.见:梅骅,陈凌武,高新主编,泌尿外科手术学,第三版,679-682.2008年.北京.人民卫生出版社.[2]. Kaya C, Akpinar IN, Aker F, et al. Large Cystitis glandularis: a very rare cause of severe obstructive urinary symptoms in an adult[J]. Int Urol Nephrol. 2007;39(2):441-444. [3]. Pantanowitz L, Otis CN. Cystitis glandularis[J].Diagn Cytopathol. 2008;36(3):181-182. [4].陈志强,叶章群,杨为民.经尿道局部电切术治疗早期腺性膀胱炎疗效观察[J].中华实验外科杂志,2004,21(12):1549-1550.[5].庄乾元,梅伟,管维,等.腺性膀胱炎治疗分析(附89 例报告) [J].中华泌尿外科杂志,2004,25:686-687.[6].曹正国,介林诸,禹平,等.经尿道钬激光和电切治疗腺性膀胱炎的疗效比较(随机对照研究) [J].中国微创外科杂志,2007,7(12),1189-1191.[7].Smith AK,Hansel DE,Jones JS.Role of cystitis cystica et glandularis and intestinal metaplasia in development of bladder carcinoma[J]. Urology,2008,71(5):915-918.[8].李宁枕,谢立平.膀胱癌诊断治疗指南.见:那彦群主编,中华泌尿外科疾病诊断治疗指南,第一版.94-166.2007年.北京.人民卫生出版社. [9]. Black PC, Lange PH. Cystoprostatectomy and neobladder construction for florid cystitis glandularis【J】. Urology, 2005,65(1):174.[10].Coelho RF, Marchini GS, Dall'oglio MF,et al. Cystoprostatectomy with ileal neobladder for treatment of severe cystitis glandularis in an AIDS patient【J】. Clinics. 2008,63(5):713-716.
温机灵 副主任医师 上海市东方医院 泌尿外科1.3万人已读 - 精选 如何准确认识腺性膀胱炎
囊性及腺性膀胱炎(Cystitis cystica et glandularis,简称CCEG)[1]是正常膀胱粘膜常见的一种粘膜增殖性改变。正常膀胱粘膜的增殖性病变最初表现为von Brunn巢,即正常的膀胱尿路上皮细胞呈巢状深入粘膜下层(见图1),细胞生长呈团状,内部并无空隙,早年有学者称之为增殖性膀胱炎。正常人大约85-95%均可见这种反应性增殖性改变。这种细胞巢可见或也可不与上皮细胞相接触(即孤立存在于粘膜下层)。随着反应性刺激的持续存在或增强,细胞巢内可出现间隙,内腔覆盖多层柱状或长柱状上皮细胞而成为腺状增生,亦称之为腺性膀胱炎(见图2);而形成囊肿间隙并有染色粉红的液体者,则称之为囊肿增生,也称之为囊性膀胱炎(见图3)。以膀胱炎作为冠名可能与该类增殖性病变多与炎症刺激有关。von Brunn巢,腺性膀胱炎及囊性膀胱炎常同时存在,也多与膀胱粘膜其他病理改变(膀胱炎症及肿瘤等)并存。自上世纪50年代初就有学者报道CCEG可能与膀胱腺癌有关,但从后来学者的分析看当时的报道仅依据一种并存现象[2],并没有之间因果关系的分析和研究。而之后很多年我们才逐渐认识到长期炎症存在与癌症的相关性。此后数十年一直有相关CCEG癌变的零星报道,也正是从上世纪50年代起,国际上多家医疗中心建议将CCEG作为癌前病变并推荐进行定期活检随访。直至发现了肠上皮化生(即肠型腺性膀胱炎),人们才确切发现了这类增殖性病变恶变的证据。而肠型腺性膀胱炎是一种比较罕见类型的腺性膀胱炎,在膀胱内呈多发,呈大滤泡状并广泛分布于以三角区为中心的膀胱各壁。其实肠型腺性膀胱炎也是与长期炎症刺激相关(尤其多见于神经源性膀胱长期留置尿管者),只是处于长期炎症刺激粘膜而使得膀胱粘膜处于临界的恶变阶段,这类腺性膀胱炎确实需要进行经尿道膀胱肿物电切术以阻止恶变的发生。但综其原因,其主要的致癌变因素还是与长期的慢性炎症刺激有关。有关炎症-粘膜增殖性病变-肠上皮化生-腺癌的关系目前以逐渐在国际上形成共识。充分认识到炎症是这类膀胱粘膜增殖性病变,甚至是发生腺癌的初始致病因素尤为重要。因此我们现在不难理解多数诊断为腺性膀胱炎的患者均有尿频尿急甚至膀胱或尿道疼痛的临床表现,其实这类患者多伴有某种膀胱炎症性疾病。对于活检发现有腺性或囊性膀胱炎,甚至肠型腺性膀胱炎电切术后需要仔细寻找炎症的病因。国际上广泛推荐采用间歇自家导尿术以代替长期留置尿管用于解决神经源性膀胱患者的排尿问题也有这方面的考虑,间歇自家导尿对膀胱刺激的程度远远低于长期留置尿管。对与病理上获得CCEG诊断的患者进行积极抗炎治疗也已在国际上形成共识[2],而这类患者获得诊断后进行膀胱灌注化疗的方法早被国际上弃用,这种局部化疗不但加重了膀胱炎症反应,明显恶化了患者尿路刺激症状,更无助于防止因长期炎症刺激导致恶变的可能性。从万方数据所能收集到的国内文献分析,我国目前针对腺性膀胱炎的诊治存在的一定的误区,多数学者仍忽略了抗炎治疗这个重要环节,仍采用对所有腺性膀胱炎进行经尿道电切术并术后膀胱灌注化疗。尽管美国克里夫兰医疗中心的学者对中国的报道产生质疑[2],可能与国外学者仅仅阅读了该文献的摘要有关。从国外作者质疑的中国文献看,中国学者还是提出了有临床意义的证据[3],如文中数据显示膀胱结石去除后腺性膀胱炎治疗的有效率高达94%,下尿路梗阻解除后有效率也高达84%,而泌尿系感染控制后腺性膀胱炎治疗的有效率为53%,能得到这些良好的结果均与明显减轻膀胱炎症有关。文中所报道的21%癌变率也是美国学者质疑的主要原因,而该文并未列出癌变患者的具体情况,也不能证明其因果关系。近年来我国学者对腺性膀胱的诊治也进行了系统的研讨,同时也认识到目前我国治疗腺性膀胱炎的现状存在一些问题,并提出了以积极寻找膀胱炎症的病因和抗炎治疗为基本原则的诊治方案[4]。本期《腺性膀胱炎电切术后膀胱灌注无菌透明质酸钠液疗效观察》一文,尽管在对腺性膀胱炎的认识和相关的定义理解上仍存在一定的误区,但作者也意识到腺性膀胱炎术后膀胱灌注化疗药物可能存在问题,并设计了随机对照研究,结果显示了针对炎症的治疗(膀胱灌注西施泰)能有效防止腺性膀胱炎的复发,为以上的观点提供了临床试验的证据,这也是本刊发表此文章的初衷,希望我国泌尿外科界能有更多的医生关注腺性膀胱炎及其相关的研究,尽早走出认识误区。图1:von Brunn细胞巢的镜下表现,粘膜下层可见巢状正常尿路上皮细胞团图2:腺性膀胱炎的病理表现,粘膜下层可见腺样结果排列的细胞团,腺腔表面被覆正常的尿路上皮细胞图3:囊性膀胱炎的病理表现,粘膜下层可见腺腔能囊状扩张的结构,表面被覆正常尿路上皮细胞参考文献1.Volmar KE, Chan TY, De Marzo AM, Epstein JI. Florid von Brunn nests mimicking urothelial carcinoma: a morphologic and immunohistochemical comparison to the nested variant of urothelial carcinoma. Am J Surg Pathol. 2003 Sep;27(9):1243-52.2.Smith AK, Hansel DE, Jones JS. Role of cystitis cystica et glandularis and intestinal metaplasia in development of bladder carcinoma. Urology. 2008 May;71(5):915-8.3.佟咸利, 宫大鑫, 刘屹立, 何忠野, 赵伟, 孙志熙及孔垂泽. 腺性膀胱炎治疗方法的探讨. 中华泌尿外科杂志. 2003;41(5):365-3674.陈志强, 马胜利及吴天鹏等. 腺性膀胱炎专题讨论. 临床泌尿外科杂志. 2003;18(1):60-62杨勇北京大学肿瘤医院泌尿外科
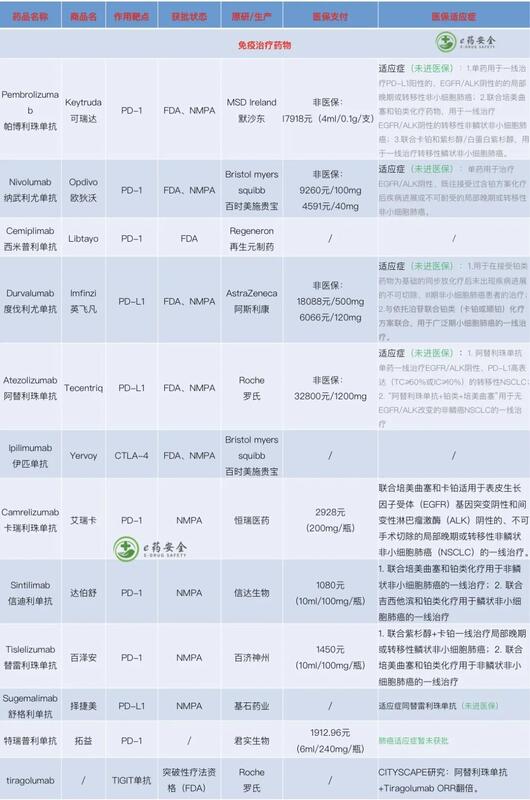
杨勇 主任医师 北京肿瘤医院 泌尿外科7人已购买 - 精选 免疫治疗-肺癌篇(PD-1/PD-L1)
对于这一最有前途的免疫治疗方法,而且被认为是解铃还需系铃人的方法。我将根据其在我国的发展轨迹以第N季,后注转载日期的方式,介绍最新的动态,并做为您关注、使用时的最新、全面的参考资料。2021.8,最新国家医保目录公布,4个国产PD-1免疫治疗药全部进医保,分别是卡瑞利珠单抗、特瑞普利单抗、替雷利珠单抗和信迪利单抗。虽然目前医保谈判的结果还没有公布,但是根据多方媒体的报道,几个进口的免疫治疗药在医保谈判中都出局了,也就是说纳武利尤单抗(O药)、帕博利珠单抗(K药)、阿替利珠单抗(T药)、度伐利尤单抗(I药)都没能进入2021年医保目录。这些药还将维持非常高的价格,患者只能通过申请慈善赠药来降低经济负担。什么是PD-1和PD-L1简单说就是针对免疫系统的免检标签。当标签存在时,免疫系统就免检放行。肿瘤表面以及与之配对的特异活性T细胞上的“免检标签”,使肿瘤能够轻松逃逸免疫系统的追杀。PD-1(programmedcelldeathprotein1)是程序性死亡受体1,是活化的T细胞表达的免疫检查点受体,是一种重要的免疫抑制分子。PD-1通过向下调节免疫系统对人体细胞的反应,以及通过抑制T细胞炎症活动来调节免疫系统并促进自身耐受。这可以预防自身免疫疾病,但它也可以防止免疫系统杀死癌细胞。PD-L1是PD-1的配体,PD-L1与免疫系统的抑制有关,可以传导抑制性的信号。肿瘤细胞也可以表达PD-L1,PD-1和PD-L1一旦结合便会向T细胞传递负向调控信号,导致T细胞无法识别癌细胞,肿瘤细胞从而实现“免疫逃逸”。PD-1可表达在T细胞、B细胞等免疫细胞表面。不过在T细胞未活化时,几乎是不表达PD-1的,仅在T细胞活化之后,PD-1才表达在T细胞表面。PD-L1除了会表达在肿瘤表面,参与免疫逃逸,还会在IFN-γ刺激下,表达在抗原提呈细胞(DC细胞、巨噬细胞等),以及血管内皮细胞的表面。图PD-1/PD-L1抑制剂重新激活T细胞阻断PD-1/PD-L1途径的治疗已经成为癌症免疫治疗的焦点。PD-1单抗和PD-L1单抗,是用来进行癌症免疫治疗的药物,PD-1单抗或PD-L1单抗阻断PD-1与PD-L1的结合,恢复T细胞肿瘤活性,激活T细胞,杀伤肿瘤细胞。一旦抗肿瘤免疫循环建立,可以产生持久的抗肿瘤效应。目前国内有多款PD-1抑制剂/PD-L1抑制剂获批上市。PD-L1抑制剂和PD-1抑制剂有什么区别药物结构不同PD-1抑制剂大多为IgG4抗体3,靶细胞为T细胞,PD-1抑制剂影响的是免疫T细胞的功能。IgG4抗体结构稳定性较差,因此几乎所有的PD-1抑制剂进行了修饰增加稳定性,不够完美的修饰,可能会导致不良反应的发生。PD-L1抑制剂大多为IgG1抗体,靶细胞为肿瘤细胞,PD-L1抑制剂影响的是肿瘤细胞。IgG1单抗是最常用的单抗,半衰期长,稳定性好。作用机制不同图4PD-1单抗的作用机制PD-1抑制剂与T细胞表面的PD-1相结合,阻断PD-1:PD-L1/PD-L2的结合,解除T细胞的活化和增值抑制,使肿瘤特异性T细胞处于活化状态,恢复T细胞的杀伤功能;PD-1抑制剂同时阻断了T细胞表面的PD-1与免疫细胞表面的PD-L1、PD-L2结合,增加潜在自身免疫反应风险。图5PD-L1单抗的作用机制4PD-L1抑制剂相比PD-1抑制剂同时结合肿瘤细胞与抗原呈递细胞表面的PD-L1,整体免疫疗效更强,恢复T细胞介导的抗肿瘤免疫作用,且不影响PD-L2的生理功能;PD-L1抑制剂具有阻断肿瘤细胞表面PD-L1与T细胞表面B7-1的结合能力,有利于全面激活T细胞;抑制剂树突状细胞表面的B7-1分子与自身高表达的PD-L1结合,因而难以结合CD28启动免疫激活,PD-L1抑制剂解除DC细胞的自我抑制,进一步强化抗肿瘤免疫应答;PD-L1单抗定向阻断PD-L1与PD-1的结合,保留巨噬细胞PD-L2的功能,避免ILD等副作用的发生5。不良反应发生率不同免疫检查点抑制剂在提高对肿瘤细胞的杀伤作用的同时,活化的T细胞攻击正常组织、自身抗体增加,细胞因子增加等诱发自身免疫炎症,产生一系列免疫治疗相关不良反应(irAEs)。与PD-1抑制剂相比,PD-L1抑制剂的3级以上不良反应事件的发生率较低3,这可能和PD-L1抑制剂还保留了PD-L2通路有关,维持巨噬细胞PD-L2的局部稳态,减少相关不良反应的发生。2019年JAMAOncol上一项Meta分析纳入125项应用PD-1/PD-L1单药的临床研究,以评估PD-1抑制剂和PD-L1抑制剂治疗相关不良反应事件的发生率,研究数据显示:接受PD-1抑制剂治疗的患者3级及以上不良反应事件发生率高于接受PD-L1抑制剂的患者(OR,1.58;95%CI,1.00-2.54)6。表1PD-1抑制剂和PD-L1抑制剂不良反应事件的发生率一项Meta分析系统性分析了23个非小细胞肺癌免疫治疗的临床研究,PD-1抑制剂12项,PD-L1抑制剂11项,研究数据显示:PD-1单抗免疫相关不良反应事件的发生率更高,(16%vs11%,p=0.07);间质性肺炎发生率:PD-1抑制剂是PD-L1抑制剂的两倍,有显著性意义(4%vs2%,p=0.01)7。近年来,以PD-1/PD-L1抑制剂为代表的免疫检查点抑制剂在肿瘤免疫治疗方面取得突破性进展,给肿瘤患者带来生存的获益。在中国,不同的PD-1/PD-L1抑制剂获批的适应症不同,患者在选择用药时,需要按照适应症和指南推荐进行合理化使用。2021年V1版《NCCN非小细胞肺癌临床诊治指南》免疫治疗1度伐利尤单抗在一线及二线免疫治疗中的应用本次更新对于免疫治疗在NSCLC一线治疗中的地位做出了较多调整。首先,对于IB期(外周T2a,N0)、Ⅰ期(中央T1abc~T2a,N0)、Ⅱ期(T1abc~2ab,N1;T2b,N0)、ⅡB(T3,N0)、ⅢA(T3,N1)患者,经治疗前评估为纵隔淋巴结阴性、N1淋巴结阳性,但医学上不可手术的患者,新版《指南》推荐进行根治性放化疗后序贯PD-L1单抗度伐利尤单抗(Durvalumab)作为巩固治疗(其中Ⅲ期患者为1类推荐,Ⅱ期患者为2A类推荐)。对于不可切除Ⅱ/Ⅲ期NSCLC(PS评分0~1)、以及2疗程及以上根治性放化疗后无进展患者的巩固免疫治疗方案,新版《指南》建议度伐利尤单抗使用剂量为10mg/kg静滴,每两周1次,至多12个月(Ⅲ期患者为1类推荐,Ⅱ期患者为2A类推荐)。本次更新还增加了一项脚注,即对于肺上沟瘤患者,推荐放疗时同时给予2周期度伐利尤单抗治疗,术后再给予2周期治疗。这一治疗方案来自于该脚注中引用的下述研究:Rusch等[24]2007年发现,患有T3~4、N0~1肺上沟NSCLC的患者在放疗(45Gy)的同时接受两个周期的铂类化疗,病情稳定或应答的患者进行开胸手术,术后再接受两个以上的化疗周期,可带来76%的R0切除率,且在56%切除标本中发现了病理完全缓解,R0切除患者的5年OS达54%。2联合免疫治疗疗法的应用值得注意的是,本次更新中,在PD-L1表达阳性(≥50%)晚期NSCLC的一线治疗中,对于腺癌、大细胞癌、非小细胞肺癌-非特殊类型(non-smallcelllungcancer-nototherwisespecified,NSCLC-NOS)患者,纳武利尤单抗+伊匹木单抗作为一线治疗由2A类推荐升级为1类推荐,且该方案对于PD-L1表达≥1%~49%的患者也升级为1类推荐;对于鳞状细胞癌,阿替利珠单抗(Atezolizumab)作为一线治疗由2A类推荐升级为1类推荐。而在继续维持治疗中,新增纳武利尤单抗+伊匹木单抗作为2A类推荐的方案(也适用于PD-L1表达≥1%~49%患者)。这是由于一篇2020年最新发表的Meta分析[25]比较了PD-L1阳性(定义为≥1%)的晚期NSCLC患者中,纳武利尤单抗(Nivolumab)加伊匹木单抗(Ipilimumab)方案(N+I)与现有其它免疫疗法(包括Pembrolizumab+铂类化疗、Pembrolizumab单药(Pem)、铂类化疗(PBC)作为一线治疗的疗效与安全性,结果显示N+I方案对PFS的延长略低于Pem+PBC方案,高于Pem、PBC单用,但是N+I方案的安全性与患者耐受性最好。TIGIT(TcellimmunoreceptorwithIgandITIMdomains),全称为T细胞免疫球蛋白和ITIM结构域蛋白,是主要在T细胞和NK细胞表面表达的免疫检查点抑制剂。PD-L1也是在免疫系统抑制中发挥作用的蛋白质。值得一提的是,TIGIT是继CTLA-4、PD-1之后新兴的免疫检查点抑制剂之一。2021年01月07日讯罗氏(Roche)近日宣布,美国食品和药物管理局(FDA)已授予TIGIT靶点新型癌症免疫疗法tiragolumab突破性药物资格(BTD),联合抗PD-L1疗法Tecentriq(泰圣奇,通用名:atezolizumab,阿替利珠单抗),一线治疗肿瘤呈现PD-L1高表达、无EGFR或ALK基因组肿瘤畸变的转移性非小细胞肺癌(NSCLC)患者。Tiragolumab是一款全人源化单克隆抗体,靶向结合于免疫细胞上的蛋白受体TIGIT。Tiragolumab作为免疫放大器发挥作用,通过潜在增强机体的免疫反应。通过与TIGIT结合,tiragolumab阻断其与一种名为脊髓灰质炎病毒受体(PVR,或CD155)的蛋白的相互作用,该蛋白可以抑制机体的免疫反应。阻断TIGIT和PD-L1可能协同实现T细胞的再活化,增强自然杀伤(NK)细胞的抗肿瘤活性。用tiragolumab和阿替利珠单抗同时阻断这两个通路有可能通过增强机体对癌细胞的免疫反应来增加抗肿瘤活性。以这种方式靶向多个免疫通路有可能在之前癌症免疫疗法进展的基础上再接再厉,扩展到疾病的早期阶段,并在高度未满足需求的领域提供新的治疗选择。基因泰克正在广泛的开发项目中调查tiragolumab的潜力,该项目建立在阿替利珠单抗观察到的获益的基础上,同时扩展到疾病的早期阶段和未满足需求的新领域。这包括在转移性NSCLC(SKYSCRAPER-01和SKYSCRAPER-06)和小细胞肺癌(SKYSCRAPER-02)中进行的随机化试验;以及在疾病早期阶段对tiragolumab的探索,包括3期NSCLC(SKYSCRAPER-03)和局部晚期食管癌(SKYSCRAPER-07)。同时tiragolumab也正在转移性食管鳞状细胞癌(SKYSCRAPER-08)和宫颈癌(SKYSCRAPER-04)中进行研究,并在其他肿瘤类型中进行早期试验。CITYSCAPE是TIGIT领域的首个随机研究,这是一项全球性、随机、双盲研究,在135例PD-L1阳性、局部晚期不可切除性或转移性NSCLC患者中开展,评估了tiragolumab与Tecentriq联合疗法、Tecentriq单药疗法用于初始(一线)治疗的疗效和安全性。该研究的共同主要终点是总缓解率(ORR)和无进展生存期(PFS),次要终点包括安全性和总生存期(OS)。结果显示,tiragolumab与Tecentriq联合一线治疗PD-L1阳性转移性NSCLC具有令人鼓舞的疗效和安全性。该研究的完整结果已在美国临床肿瘤学会(ASCO)2020年虚拟科学会议上公布。具体数据为:(1)中位随访10.9个月,在意向性治疗(ITT)患者群体中,与Tecentriq单药治疗相比,tiragolumab+Tecentriq联合治疗同时达到了2个主要终点:总缓解率(ORR)显著提高(37%vs21%)、疾病恶化或死亡风险显著降低42%(中位PFS:5.6个月vs3.9个月;HR=0.58)。(2)对PD-L1高表达(TPS≥50%)患者开展的一项探索性分析显示:与Tecentriq单药治疗相比,tiragolumab+Tecentriq联合治疗显著提高ORR(66%vs24%)、将疾病恶化或死亡风险显著降低70%(中位PFS:未达到vs4.11个月;HR=0.30,95%CI:0.15-0.61)。(3)该研究中,tiragolumab与Tecentriq联合治疗具有良好的耐受性,所有3级或以上全因不良事件(AE)的发生率方面,联合治疗与Tecentriq单药治疗相似(48%vs44%)。中国信达生物研发的TIGIT抗体IBI939在中国获得临床试验默示许可,适应症为:晚期肿瘤(血液肿瘤和实体瘤)。这是首个在中国国内获批临床的TIGIT抑制剂。Pegilodecakin是目前处于临床研究中的一种新型药物,与PD-1免疫药物Pembrolizumab或Nivolumab联合,显示出良好的安全性,并表现出具有前景的疗效,有望为非小细胞肺癌和肾癌患者带来新疗法。Pegilodecakin由重组白介素10(IL-10)组成,IL-10与聚乙二醇(PEG)分子“黏”在一起。IL-10与聚乙二醇黏在一起后,“个头”增大,从而阻止或延迟其分解,以便延长在人体内循环的时间,“作战”时间更长久。IL-10是一种调节各种免疫细胞活性的蛋白质,高浓度的IL-10可以激活针对癌细胞的免疫反应。Pegilodecakin如何与PD-1药物协作?CD8+T细胞的“强项”是识别和破坏癌细胞,Pegilodecakin通过刺激CD8+T细胞的存活、增殖和“杀伤”潜力而发挥作用。研究人员认为增加肿瘤内CD8+T细胞的数量可以改善患者的预后和生存。PD-1药物可以解除对T细胞的抑制,Pegilodecakin可以刺激免疫细胞增强杀伤力,二者相辅相成。这就像PD-1药物把被困的士兵解救出来,Pegilodecakin负责把这些士兵培养成精兵强将,战斗力自然就增强了。2021.12,中临善募研究中心正在招募EGFR突变非小细胞肺癌患者。3免疫治疗前病理评估和治疗后监测对于分子检测PD-L1&#60;1%及阴性患者的系统治疗,本次更新明确了将患者根据病理类型分为两类,第一类包括腺癌、大细胞癌、NSCLC-NOS,而第二类包含鳞状细胞癌患者,两类患者接受的系统性初始治疗方案略有差异。同时,还对于患者疗程中的监测增加了两条脚注:其一是一线治疗期间的监测应在2疗程后进行治疗应答评估,随后每2~4疗程对已知病灶进行CT/增强CT评估,或在临床指定时进行评估;其二是后续治疗期间的监测,应每6~12周对已知病灶使用CT或增强CT进行应答评估。本次更新还增加了关于PD-1/PD-L1抑制剂治疗的禁忌证,可能包括活动性或先前记录的自身免疫性疾病和/或当前使用免疫抑制药物,或存在致癌驱动基因突变(例如EGFR外显子19缺失、外显子21p.L858R点突变、ALK重排等),此类患者预测将缺乏获益。PACIFIC研究数据:2017年PACIFIC数据首次在欧洲肿瘤学年会(ESMO)上公布:相比于安慰剂,I药延长了3倍的无疾病进展生存期(PFS):16.8个月VS5.6个月,降低了48%的疾病进展或死亡的风险。同年,数据发表于《新英格兰医学杂志》[1],堪称重磅级学术炸弹!也是基于这一结果,I药被FDA批准用于以铂类药物为基础的放化疗后未出现疾病进展、不可切除的Ⅲ期NSCLC的治疗。2018年世界肺癌大会(WCLC),PACIFIC临床试验的OS数据公布:I药组1年、2年的生存率为83.1%、75.3%;而安慰剂组1年、2年的生存率为66.3%、55.6%。当时,根据官方的预测I药组OS至少有40个月左右,该研究结果也再次发表在《新英格兰医学杂志》[2]。2019年美国临床肿瘤学会(ASCO)年会,PACIFIC研究公布了新的研究成果:I药组3年OS率达到57%,对比安慰剂组的43.5%,I药的3年OS率提高13.5%[3]。OS依然未达到,研究继续。2020年欧洲肿瘤医学协会(ESMO)年会,终于等到PACIFIC研究的中位OS数据——47.5月,四年生存率49.6%中位OS高达47.5月,4年OS率达到了49.6%,对比安慰剂的36.3%,I药将4年OS率提高了13.3%目前,I药已在国内上市,用于在接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除、III期非小细胞肺癌(NSCLC)患者的治疗。中国非小细胞肺癌免疫检查点抑制剂治疗专家共识(2019年):中国肺癌杂志2020年2月第23卷第2期ChinJLungCancer,February2020,Vol.23,No.2免疫检查点抑制剂(immunecheckpointinhibitors,ICIs),尤其是以程序性死亡因子-1(programmeddeath-1,PD-1)/程序性死亡因子配体-1(programmeddeath-ligand1,PD-L1)为靶点的ICIs在驱动基因突变阴性的NSCLC治疗中取得了突破性的进展,为患者带来了生存获益,改变了NSCLC的治疗格局,显示出越来越重要的地位。治疗推荐:一线高表达一级推荐除单药外,帕博利珠单抗联合含铂双药化疗,对于PD-L1高表达患者可带来更显著的获益。驱动基因敏感突变阳性NSCLC。IMpower150是第一个采用ICIs在EGFR/ALK突变患者中显示出有临床获益的随机III期研究。在贝伐+化疗的标准基础上增加ICIs,对于EGFR/ALK突变的晚期NSCLC患者,该方案有可能成为一种新的治疗选择。可预测疗效的生物标志物PD-L1表达:目前认为肿瘤组织PD-L1的表达是抗PD-1/PD-L1治疗前选择优势人群比较合理的标志物。尤其是晚期NSCLC的免疫治疗疗效预测的生物标志物之一。PD-L1表达水平的评价标准包括:CPS评分、TPS评分、IPS评分等。不同的癌种适应症,选择的评价标准有所不同,有的选择TPS评分,有的选择CPS评分,也有的选择IPS评分,其中TPS和CPS评分最常用。下面来分别阐述说明:TPS评分,指的是:肿瘤细胞阳性比例分数(TumorProportionScore,TPS)。目前PD-L1检测关注的焦点是肿瘤细胞的PD-L1表达水平,其表达水平的高低会直接影响到免疫检查点抑制剂治疗效果。注意:TPS是一个百分比,通常以1%、50%为分界线,其表达阳性的cutoff值判定为:TPS&#60;1%、TPS≥1%-49%、TPS≥50%?CPS评分,指的是:联合阳性分数(综合阳性评分,CombinedPositiveScore,CPS)。除了肿瘤细胞表达PD-L1之外,淋巴细胞、巨噬细胞等免疫细胞以及间质细胞也会有PD-L1表达,从而抑制免疫功能。为此引入另一个评价PD-L1表达水平的概念,这就是CPS!注意:CPS是一个数值,不是百分数。不同癌种,CPS评分标准的界限cutoff值不同,也就是说,官方批准的免疫治疗用于不同癌种,是基于不同的CPS评分值,有的是以CPS≥1,有的是以CPS≥10,比如FDA批准Pembrolizumab联合化疗治疗PD-L1表达阳性(联合阳性评分CPS≥10)的局部复发性不可切除或转移性三阴性乳腺癌。?CPS和TPS的主要不同点在于:1、是否计算肿瘤区域阳性表达的免疫细胞数量,CPS不局限于肿瘤细胞PD-L1表达,还包括相关免疫细胞PD-L1表达;2、TPS为百分比数值,CPS是百分制数值。IPS评分,仅将肿瘤相关的免疫细胞(淋巴细胞、巨噬细胞等)PD-L1表达情况作为单独评价指标用来区分获益人群。比如,Atezolizumab获批用于尿路上皮癌和肺癌时用的就是IPS指标。肿瘤基因突变负荷(tumormutationalburden,TMB)/血液肿瘤基因突变负荷(bloodtumormutationalburden,bTMB):目前研究显示TMB/bTMB作为ICIs治疗效果的预测标志物尚存在较大争议。错配修复缺陷(mismatchrepairdeficient,dMMR)或微卫星不稳定-高(microsatelliteinstability-high,MSI-H):MMR状态虽然有可能用于预测PD-1/PD-L1抑制剂的疗效,但由于其在肺癌中的发生率很低,dMMR/MSI-H对肺癌免疫治疗疗效的预测价值还需要更多的研究和数据来验证。免疫治疗的评估2017年初,RECIST工作组正式提出实体肿瘤免疫疗效评价标准(ModifiedRECIST1.1forimmunebasedtherapeutics,iRECIST)[30],iRECIST标准引入了即待证实的疾病进展(immuneunconfirmedprogressivedisease,iUPD)和已证实的疾病进展(immuneconfirmedprogressivedisease,iCPD)的概念,而将之前RECIST1.1标准评定的PD暂视为iUPD,依据患者的肿瘤类型、疾病分期和临床情况综合判断是否继续治疗,在4周-6周进行再次评估以确认iCPD。在此评价模式下,iUPD之后可分别出现病情稳定(immunestabledisease,iSD)、部分缓解(immunepartialresponse,iPR)或免疫完全缓解(immunecompleteresponse,iCR)等几种可能,只要iCPD未得到证实,就要循环持续评价并记录未证实的原因。iRECIST标准提出了循环反复评价的模式,一定程度上可捕获免疫治疗时代下非典型缓解类型(如假性进展和延迟反应)的出现。NSCLC患者接受免疫治疗时,可能会发生13%左右的不典型应答,其中包括假性进展和分离性应答,这些患者的OS明显优于真正确认为PD的患者。约11%接受免疫治疗超过6个月患者可能被RECIST1.1标准评价为PD,其实却能够从治疗中获益[31]。免疫治疗超进展(hyperprogression,HP)HP是相对于通常的进展而言,HP被定义为肿瘤反常的加速生长,包括:①在ICIs治疗后第一次评价时出现进展,或至治疗失败时间(TTF)2个月;②肿瘤体积增加&#62;50%;③肿瘤增长速度(TGR)增加&#62;2倍。目前关于HP的机制尚不明确。HP可发生于ICIs治疗过程中任何阶段,且无明确的预测指标,初步估计达10%,对于老年患者更需关注。尚未发现HP与肿瘤负荷、肿瘤类型、治疗线数、PD-L1表达水平之间存在相关性。发生HP的患者总体预后较差,OS仅为3个月-4个月;一旦出现HP的症状,需尽早由免疫治疗转为抢救化疗[42,43]。免疫治疗所特有的不良反应即免疫相关不良反应(immune-relatedadverseevents,irAEs)CTLA-4抗体引起的irAEs比较广泛、发生率较高,特异性较小,毒性较强。抗PD-1/PD-L1抗体在T细胞反应后期(免疫效应阶段)发挥作用,主要多激活外周组织中的T细胞(如肿瘤微环境),因此引起的irAEs比较局限,发生率较低,特异性较强,毒性相对弱。相对禁忌证。已有对特殊人群中应用ICI的一些研究,提示:1)对于合并自身免疫病的患者,如果病情已经控制得当,接受PD-(L)1抗体治疗相对安全。但对于病情尚未控制的人群,则大概率会加重病情,需要综合权衡治疗选择;2)年龄>70岁并不是使用PD-(L)1抗体的禁忌证。单纯的高龄可能并不显著影响PD-(L)1抗体的疗效和安全性。但体力与体能状态较差的患者接受PD-(L)1抗体治疗后生存期可能会缩短;3)已有研究表明基线时使用皮质类固醇(≥10mg泼尼松)与免疫治疗疗效相关,其中14%患者在PD-1治疗前开始接受皮质类固醇治疗,总生存和无进展生存明显变差。故《专家共识》建议在开始免疫治疗时谨慎使用皮质类固醇,除非必须进行激素治疗;4)HIV感染患者多种肿瘤的发生率明显提高。对于病情基本控制的HIV感染患者来说,使用PD-1抗体的疗效和毒副作用与非感染患者基本相似。5)出现严重治疗反应患者。irAEs恢复后再次接受免疫治疗的原则影响患者再次使用ICIs的关键因素取决于末次irAEs出现的程度、患者的一般状况以及是否存在其它治疗模式。如果二级irAEs的症状和/或实验室指标降至一级或以下,可以考虑再次使用ICIs,但是需要谨慎使用,特别对于出现早发irAEs的患者,不推荐剂量调整。严重irAEs缓解后,患者再次接受ICIs治疗,irAEs可能再次出现;如果再次出现irAEs,则这类ICIs应永久停用。目前,PD-1类抗癌药虽好,价格却让人咋舌:每位患者一年的治疗费用(未包含赠药费用),O药约为44万元,K药约为61万元,拓益约为19万元,达伯舒约为27万元。度伐利尤单抗注射液Durvalumab,PD-L1抑制剂,AstraZenecaUKLimited(英国),用法2支:3万6/月。免疫治疗需维持时间尚资料较少,个别研究结果提示我们,1年的免疫治疗时间可能是不够的。其结果也存在商业目的可能,最终结论期待更多研究。在研药一觅替雷利珠单抗是目前唯一对Fc段进行了特殊基因工程改造的PD-1单抗,也是目前全球第二个、国内第一个全面获得一线鳞状及非鳞状非小细胞肺癌(NSCLC)III期注册临床研究成功的PD-1抗体,同时在小细胞肺癌(SCLC)领域的研究也取得了初步成效,显示出良好的应用前景。中国医学科学院肿瘤医院胸外科开展的术前新辅助免疫治疗研究汇报了信迪利单抗在术前新辅助治疗可切除的鳞状NSCLC的研究结果。该试验共纳入了40例可切除的I-IIA期患者。,在术前接受两周期的信迪利单抗治疗,手术在免疫治疗后第29-43天进行。根据RECIST1.1标准,8例患者获得影像学上的部分缓解(PR),整体ORR为20%。15例患者(40.5%)出现显著病理学缓解(MPR,&#60;10%的活肿瘤细胞),其中6例(16.2%)出现完全病理缓解(pCR)。病理学缓解与患者PCT检查肿瘤组织标准摄取值(SUV)下降有直接关系。在SUV下降>30%的9例患者中,8例有MPR,而SUV≤30%以下的11例患者无MPR反应。其它对于晚期NSCLC患者,帕博利珠单抗单药的研究显示:大样本32758(PS评分为0-1)/39199例,对于PD-L1≥50%的这部分患者,5年OS率更是达到25%。后线接受免疫治疗5年的OS也达到15.5%。另112例较弱(PS评分为2)的研究显示:患者的整体临床获益率为37%,一线及后线接受帕博利珠单抗治疗的临床获益率分别为38%和36%。随着PD-L1表达水平增加,临床获益率逐渐升高;PD-L1表达为<1%、1-49%及≥50%患者的临床获益率分别为22%、47%和53%(图2)。2019年肺癌NCCN指南发布,治疗理念多处更新1、PDL1单抗durvulumab作为III期不可切除非小细胞肺癌同步放化疗后的维持治疗,推荐力度从2A升至1级。将低毒长效的PD1单抗作为维持治疗成为一种新的发展趋势,I类的推荐级别提示临床医生对于III期不可手术肺癌患者可充分考虑durvulumab的序贯维持。重磅研究PACIFIC显示,对不可切除III期NSCLC同步放化疗之后应用度伐利尤单抗(PD-L1;阿斯利康公司)进行巩固治疗,3年生存率达到57%,对照组为43%,显著提升了生存率,彻底改变了III期NSCLC的生存情况,该研究的方案也已经成为国际上公认的标准治疗方案。2、在晚期初治的非小细胞肺癌的治疗分群时,除了进行基因检测(EGFR、ALK、ROS1、BRAF)外,PDL1的检测推荐力度从2A级升至1级。也将后续所有人群的治疗分为三大类:(1)基因突变靶向治疗患者;(2)PDL1≥50%免疫治疗群;(3)靶向免疫均不受益的传统放化治疗群。进一步肯定了免疫治疗在一线中的治疗地位。医患朋友也应进行三方面的划分。备注:PD1免疫治疗作为EGFR/ALK突变肺癌靶向耐药后不论PDL1表达如何的二线治疗,并不是很有效。3、对于PDL1≥50%的初治晚期非小细胞肺癌患者,此处主要有三大更新:(1)初治晚期NSCLC患者想要一线使用免疫治疗,除了要满足EGFR/ALK阴性,PDL1≥50%外,指南又添加了新的备注,即患者不能具有与免疫治疗想冲突的特征如有活动性或之前记录在案的自身免疫性疾病,和或正在使用免疫抑制性药物。或者患者具有不适合免疫治疗的突变基因。(2)在PDL1≥50%的非鳞非小细胞肺癌患者中,除了keytruda单药可以使用外,还推荐了pem+培美曲赛+顺铂/卡铂方案以及贝伐单抗+阿特朱单抗+多西他赛+卡铂的方案。相对应的维持治疗也有对应的方案。虽然联合化疗的方案疗效更高,但是单药K药方案仍然是优先选择的。(3)对于PDL1≥50%的鳞癌患者的一线方案,除了K药单药外,pem联合紫杉醇/白蛋白结合型紫杉醇+卡铂/顺铂也被推荐,但单药K仍是优先推荐。4、在PD1或PDL1单抗治疗进展后,转换为其他的PD1/PDL1药物并不做常规推荐。5、TMB首次与其他驱动基因MET14、RET、HER2一起成为有助肺癌治疗的有临床价值的标记物。2A类推荐。但是也明确指出现在的TMB检测的弊端,即虽然TMB有助于识别适合免疫治疗肺肺癌患者,但目前对于TMB的评价标准并不统一。总之(1)免疫方面进展更多,III期维持、一线推荐、TMB进入标志物行列都具有重要意义(2)基因检测方面,血检推荐顺序的提前以及TMB的新标志物的添加都代表NGS二代检测以及血检的崛起,得到学术界的逐步认可(3)2019年刚刚开始,基于PD-1/PD-L1的免疫治疗研究成果热度超越靶向治疗,表达大于50%的病例己可做为首选治疗。12月17日,首个国产PD1特瑞普利单抗上市。PD-1/PD-L1免疫疗法是当前备受全世界瞩目、正掀起肿瘤治疗的革命,引领癌症治疗的变革,为患者带来新的希望的新一类抗癌免疫疗法,旨在充分利用人体自身的免疫系统抵御、抗击癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力,实质性改善患者总生存期。与传统疗法相比,免疫疗法最大的优势之一,就是疗效具有持久性。比如,在黑色素瘤里,欧美20%左右的晚期患者能实现临床治愈,成为“超级幸存者”,这是免疫疗法带来的生命奇迹。全球肿瘤专家对免疫药物感到无比兴奋,有几个最大的原因:1:它有更广谱的抗癌效果(O药已经在全球获批治疗9个癌种,k药获批9个癌种)。2:它比化疗的整体副作用要小得多。3:它如果起效,可能让晚期患者长期存活,甚至临床治愈,这是免疫药物区别于其它所有药物最大的不同。PD-1/PD-L1目前,全球上市的免疫检查点抑制剂PD-1或PD-L1抑制剂共6个,以后……O药:Opdivo(Nivolumab)、K药:Keytruda(Pembrolizumab)、T药:Tecentriq(Atezolizumab)、I药:Imfinzi(Durvalumab)、B药:Bavencio(Avelumab)。近两日让癌友圈振奋的好消息是O药和K药都以正式运抵中国,并且O药在国内的价格也已全面公布,中国的患者终于迎来了真正的免疫治疗元年!全球肿瘤医生网医学部将药物用药信息总结如下,供癌症患者参考。关于PD-1患者关心的六大问题一、副作用的处理PD-1抑制剂,总体的副作用远小于传统的放化疗。最常见的副作用是“流感”样的表现:发热、乏力、头晕、全身肌肉酸痛、嗜睡等,发生率在30%左右,对症处理即可。肺部问题(肺炎):新发或恶化的咳嗽;胸痛;气短。肠道问题(结肠炎):可能导致肠道内的炎症或穿孔。包括:腹泻或排便次数多于平常;便血和腹部严重(腹部)疼痛或压痛。肝病(肝炎):皮肤或眼睛变黄;严重恶心或呕吐;腹部右侧的疼痛(腹部);嗜睡;尿黄(茶色);皮肤容易出血或瘀血;常有饥饿感。内分泌问题(特别是甲状腺,垂体,肾上腺和胰腺):激素腺体不能正常工作,包括:持续头痛或不寻常的头痛;极度疲劳,体重增加或减少;眩晕或昏厥;情绪或行为的变化,如性行为减少,烦躁或健忘;脱发、感冒、便秘;声音改变、口渴或尿多。肾脏问题:包括肾炎和肾衰竭。包括:尿量减少;尿液中的血液、脚踝肿胀和食欲不振。皮肤问题:这些问题的迹象可能包括:皮疹、瘙痒、皮肤起泡和口腔或其他粘膜中的溃疡。大脑炎症(脑炎):包括:头痛、发热、疲倦或虚弱混乱、记忆问题、嗜睡、幻觉、癫痫发作。其他器官的问题:视力的变化;严重或持续的肌肉或关节疼痛和严重的肌肉无力。严重的输液反应:发冷或寒战、瘙痒或皮疹、呼吸困难、头晕、发热。使用pd-1治疗,慎用异体干细胞移植并发症。这些并发症可能很严重,可能导致死亡。此外,大约5%-10%的患者,会出现严重的免疫相关的炎症反应:甲状腺炎症(表现为甲亢、甲减、或先甲亢后甲减)、免疫性肺炎、免疫性肠炎、免疫性肝炎、甚至免疫性心肌炎。免疫性炎症,如果发现不及时,处理不到位,偶尔发生致命的事故。对于甲状腺问题,可以请内分泌科医生会诊。甲亢可以服用抗甲状腺药物,甲减可以补充优甲乐。对于免疫性炎症,如肺炎、肝炎、肠炎等,需要酌情加上口服或静脉的糖皮质激素,如地塞米松、泼尼松、甲强龙等,对于病情较重的,还需要加上环磷酰胺、霉纷酸脂等免疫抑制剂。对于发生细胞因子风暴的患者,需要及时使用IL-6抗体,托珠单抗。二、PD-1抑制剂的疗效如何?在绝大多数、未经挑选的实体瘤中,单独使用PD-1抑制剂的有效率,其实并不高:10%-30%左右。唯一的例外,是经典型霍奇金淋巴瘤,有效率突破60%以上。PD-1抑制剂有效率偏低,为何学术界和癌友圈还如此疯狂和痴迷呢?主要的原因是:PD-1抑制剂疗效的持久性。由于免疫系统具有记忆功能,因此一旦PD-1抑制剂起效,其中部分病友实现临床治愈,也就是说五年、十年不复发、不进展、长期生存。尤其是较早的恶性黑色瘤、肾癌以及非小细胞肺癌中,都已经观察到了类似的现象:PD-1抑制剂的出现,将晚期恶性黑色素瘤和晚期非小细胞肺癌的生存率提高了数倍:晚期恶性黑色素瘤的5年生存率从15%左右,提高到了35%上下;而晚期非小细胞肺癌的5年生存率从5%左右,提高到了15%上下!此外,通过联合治疗,把原来不适合PD-1抑制剂治疗的病人,转化为可以从中获益的人群也可以提高治疗效果。目前,PD-1抑制剂主流的搭档有如下几个:(1)联合另一个免疫治疗药物:PD-1抑制剂联合CTLA-4抗体,已经被批准用于恶性黑色素瘤;在肾癌、TMB高的非小细胞肺癌中三期临床试验已经成功。此外,IDO抑制剂、TIM-3抑制剂、LAG-3抗体等新型的免疫治疗新药,正在研发中。(2)联合化疗:PD-1抑制剂联合化疗,已经被批准用于晚期非鳞非小细胞肺癌一线治疗;类似的方案,用于胃癌、肠癌、三阴性乳腺癌等也有不错的初步数据。(3)联合放疗:PD-1抑制剂联合放疗,在肺癌、恶性黑色素瘤等肿瘤中,已有不错的数据;回顾性研究甚至提示,放疗联合PD-1抑制剂,可以将生存期提高数倍。(4)联合靶向药:PD-1抑制剂联合抗血管生成的靶向药(贝伐、阿西替尼、乐伐替尼、卡博替尼等),已有不错的初步数据;但联合EGFR抑制剂(如易瑞沙、特罗凯、凯美钠、阿法替尼、泰瑞沙等),需要当心,可能发生严重的副作用。(5)联合溶瘤病毒:PD-1抑制剂联合溶瘤病毒T-VEC,在恶性黑色素瘤中,有效率超70%,完全缓解率突破30%,非常有前景。在其他肿瘤中,多种溶瘤病毒正在研发中。(6)联合个性化肿瘤疫苗:基于肿瘤基因突变所产生的新生抗原(neoantigen),可以设计和合成多肽或RNA疫苗。PD-1抗体联合这类私人订制、个性化肿瘤疫苗,已经有初步的成功经验,可以预防肿瘤复发,可以初步临床治愈晚期肿瘤。(7)联合特异性肿瘤免疫细胞治疗:PD-1抑制剂联合CAR-T等新型的特异性肿瘤免疫细胞治疗,在血液肿瘤中,已有初步的、不俗的数据。三、如何预测PD-1的效果?PD-1抑制剂在未经选择的实体瘤患者中,有效率只有10%-30%;究竟哪些患者能够最终获益,医学人员仍在不断研究,目前主要的评价指标有以下四个供临床医生参考:(1)PD-L1表达PD-1与PD-L1如同一对“情侣”,其中PD-1位于免疫细胞的表面,而PD-L1则位于肿瘤细胞的表面。这对“情侣”一旦结合,负责杀伤肿瘤细胞的免疫细胞就会把肿瘤细胞当作“朋友”,从而不再对其进行攻击。研究发现,当肿瘤细胞表面有PD-L1的表达,那么使用PD-1抑制剂或者PD-L1抑制剂抑制肿瘤的概率就会增加,所以,肿瘤组织中PD-L1的表达情况,就成为预测PD-1/PD-L1抑制剂有效率的一个指标。在非小细胞肺癌的临床实验中,人们发现,如果肿瘤组织中PD-L1的表达率超过50%,PD-1抑制剂可以作为首选治疗方法治疗肿瘤,而如果PD-L1的表达率>1%,免疫检查点抑制剂可以使一线化疗失败的肺癌患者获益。(2)MSI(微卫星)检测微卫星不稳定性是我们身体中基因的一种病态情况,与肿瘤的发生密切相关。研究表明,如果肿瘤组织中微卫星处于高度不稳定的状态,即MSI-H,使用PD-1抑制剂的有效率高于微卫星不稳定性低的状态(MSI-L)和微卫星稳定的状态(MSS)。所以,MSI-H就成为了预测PD-1抑制剂的一个重要的生物标志物。(3)肿瘤基因突变负荷(TMB)检测肿瘤突变负荷高,从免疫治疗中获益的概率就大。在CheckMate-032临床研究中,按照TMB高低划分成TMB高、TMB中、TMB低三类病人,在接受联合治疗的人群中,三组的有效率分别为62%、20%、23%;而三组的中位总生存期,分别为:22.0个月、3.6个月、3.4个月——22.0个月与3.4个月,相差6倍!所以,TMB也是预测PD-1抑制剂的一个重要的生物标志物指标。(4)肿瘤浸润淋巴细胞(TIL)检测通过免疫组化染色(CD3、CD4、CD8等),可以看出肿瘤组织中是否有较多的淋巴细胞浸润。浸润的淋巴细胞越多,PD-1抑制剂的有效率越高。四、如果PD-1起效,到底应该用多久?目前国内外,标准的方案是:手术或同步放化疗后,巩固性、辅助性使用的病友,PD-1抑制剂建议用满1年;而晚期的、全身转移的病友,建议用满2年。然而,越来越多的证据支持,使用PD-1抑制剂满6个月,且肿瘤缩小达到完全缓解、部分缓解(肿瘤缩小超过30%以上)的病友,可以再巩固2-3次后,酌情停药或调整剂量和间隔。五、PD-1耐药后应该怎么办?PD-1抑制剂有效的病人,一般疗效持久;但是,目前已经观察到30%左右的患者,出现了疾病的耐药。克服耐药的关键,主要是两点:首选,如果可能,可以通过对新增的或者不断增大的耐药部位,进行穿刺活检和深入的免疫分析,找到耐药的原因,根据原因治疗。比如,有的病人是由于TIM-3、LAG-3或IDO代偿性高表达;那么选择,PD-1抑制剂联合TIM-3抑制剂、LAG-3抗体、IDO抑制剂,就是最好的治疗方案。其次,对于不能明确耐药原因的病友,可以结合具体病情,选择最佳的联合搭档,逆转耐药,延长生存期;或者,更换为放化疗、介入、射频、粒子植入等传统治疗。六、使用PD-1,患者需要注意哪些问题?首先,如下病人不适合、不建议尝试PD-1抑制剂:病情进入终末期、卧床不起的病人;有急性细菌感染,尚未控制的病人;做过肝移植、肾移植的病人;有系统性红斑狼疮、白塞病、干燥综合征、血管炎等自身免疫病,尚未控制的病人;携带MDM2扩增、EGFR突变、JAK突变等病人等(有些患者可以首选靶向治疗)。其次,使用PD-1抑制剂前,一般建议完善如下检查,基本正常,然后再使用:血常规、肝肾功、电解质、凝血、甲状腺功能,心电图、腹部B超、胸部X线。最后,也是最重要的一点:越来越多的证据支持,PD-1抑制剂这类免疫治疗,应该在患者一般情况比较好,肿瘤负荷比较小的时候,尽早用。附:PD-1,PD-L1的前世/今生/未来近几年在癌症领域一夜之间多了一种治疗方案,叫“PD(程序死亡性受体)-1/PD-L1免疫疗法”。肿瘤免疫治疗是应用免疫学原理和方法,提高肿瘤细胞的免疫原性和对效应细胞杀伤的敏感性,激发和增强机体抗肿瘤免疫应答,协同机体免疫系统杀伤肿瘤、抑制肿瘤生长。通俗一点我们体内,癌细胞就像揭去封印的小恶魔,不再受人体的控制。一个变两个,两个变四个,四个变八个……癌细胞的特点就是失控性生长。但是,人体免疫系统也不是白吃饭的。它就像是人体的铁甲卫士,专门负责截杀各路侵入人体的细菌、病毒等(比如细胞毒性T细胞,它是一种白细胞,能够侦查到被感染或发生突变的细胞)。当他发现这些细胞后就会发出毒素,启动其自毁程序(细胞程序性死亡)。但T细胞这样玩命一路杀到底,杀红了眼,人挡杀人,佛挡杀佛,最后会把正常的健康细胞也杀死。所幸,激活一种名叫PD-1的分子,就可以关掉T细胞,使得正常细胞免受攻击。也就是说,有了PD-1,T细胞就不会攻击正常细胞。但聪明的癌细胞也会表达PD-L1受体,和T细胞表面的PD-1结合,来迷惑T细胞。当PD-1和PD-L1结合之后,T细胞遇见肿瘤细胞就会手下留情,非但不会杀死肿瘤细胞,甚至让肿瘤细胞继续在人体内休养生息。这该怎么办呢?聪明的研究者们想到,只要阻止PD-1和PD-L1的结合就可以了。因此,他们研究出了分别跟这两个受体结合的抗体。一种与T细胞表面的PD-1结合,使其重振往日雄风。另一种抗体与肿瘤细胞表面的PD-L1结合,让肿瘤细胞无法再迷惑T细胞。最终,T细胞围剿各种肿瘤细胞,大获全胜。而这,就是我们常说的PD-1/PD-L1免疫疗法。前世篇—CTLA-4说到PD-1抑制剂,不得不提到CTLA-4抑制剂Yervoy?才是全球首个免疫检查点药物。聊起CTLA-4抑制剂Yervoy?,可以说全是眼泪,如果当年BMS没有延缓CTLA-4的药物研发,或许PD-1抑制剂OPDIVO早10年就上市了。故事是这样说的:法国人PierreGoldstein在1987年无意中发现了T细胞上的一个分子CTLA-4,起初大家对这一分子并不在意,而纽约纪念斯隆凯特琳癌症中心的JamesAllison教授却敏锐地意识到CTLA-4可能在肿瘤免疫里具有“非同凡响”的功能。JamesAllison算是开启了通过抑制免疫检查点的途径来治疗癌症的肿瘤免疫治疗新篇章。(所以Allison是癌症免疫治疗的先驱,估计很大可能会拿诺贝尔奖哟~)BMS开始研究CTLA-4蛋白分子对抗癌症的影响,可惜后来他们发现这只是一点曙光而已,因为这个分子是在T细胞上,而其配体(ligand)并不具备肿瘤特异性,阻断CTLA-4会激活全身免疫系统,副作用太强。这时候遗憾的事情发生了,BMS公司在投入免疫疗法研发方向近十年之后失去了耐心,因为看不到大的希望,于1997年决定将西雅图研发部门关掉。某种程度上说,BMS公司当年对这一方向的不重视,某种程度上是拖延了免疫检查点药物的开发,否则这一类药物可能会早个10年问世。不过好在2009年,BMS公司通过收购Medarex获得了ipilimumab。最终,美国FDA于2011年3月25日批准CTLA-4抑制剂ipilimumab(商标名称为Yervoy?)用于治疗晚期黑色素瘤。今生篇—PD-1/PD-L1免疫疗法除了CTLA-4以外,科学家陆陆续续发现了近十个免疫检查点,发现了真正具有肿瘤特异性的一个蛋白分子,也就是现在闻名天下的PD-1,从而掀起了验证通过抑制PD-1(或者PD-L1)是否能抗癌的研究新方向。BMS公司研发的Opdivo最早于2014年7月在日本获得批准,是全球第一个获批上市的PD-1/PD-L1药物。2014年12月,Opdivo美国获批准上市。不得不说上帝还是眷顾BMS公司的。说了这么辛酸史,肯定有人还是会问究竟PD-1/PD-L1究竟为什么会有这么大的魔力会激起科学家、医生和病友们如此大的兴趣呢?持久性:对PD-1抑制剂有效的病人,疗效维持的平均时间较长,部分病友甚至维持了五年、十年。PD-1抑制剂的出现,让恶性黑色素瘤、肺癌、肾癌等多种肿瘤的生存时间明显延长,5年生存率甚至翻倍。对于那些使用PD-1抑制剂达到完全缓解、疗效维持时间超过5年的幸运儿,不少乐观的医生甚至认为这部分人已经被“临床治愈”,这是肿瘤医学史上,开天辟地、从未有过的。广谱性:PD-1抑制剂,目前看来,对于绝大多数肿瘤,都是可以尝试的。目前临床试验以肿瘤突变负荷高,微卫星不稳定的肿瘤为主,包括黑色素瘤、肺鳞癌、肺腺癌、小细胞肺癌、胃肠道肿瘤、头颈癌、肝癌等。低毒性:PD-1抑制剂毒副作用,相对于传统的放化疗等治疗要小的多,3~4级严重不良反应的发生率,降低了一半甚至更多。现在我们再来扒一扒目前世界上,还有哪些PD-1/PD-L1已经上市:Keytruda由默沙东公司开发,是美国FDA批准的第一个PD-1免疫检测点抑制剂。2015年,美国前总统卡特晚期黑色素瘤在Keytruda的作用下,神奇消失;在今年结束的美国临床肿瘤学会(ASCO)年会上,Keytruda更是展现了治疗多种癌症的潜力。罗氏的Tecentrip(Atezolizumab)于2016年5月获批用于尿路上皮癌(膀胱癌),是全球第一个上市的PD-L1抑制剂。2016年10月被批准用于治疗靶向药、化疗失败的非小细胞肺癌患者。2017年3月,美国FDA宣告同意由德国默克公司与辉瑞一起研制的免疫疗法新药Bavencio上市,用于治疗梅克尔细胞癌(MMC,一种稀有肿瘤),Bavencio成为全球第四个PD-1/PD-L1抗体药物2017年5月,PD-1/PD-L1抑制剂竞技场迎来了第五名玩家,阿斯利康PD-L1单抗Imfinzi获得美国FDA加速批准,用于治疗晚期或转移性尿路上皮癌。目前全球上市的5个PD-1/PD-L1抑制剂均属于大分子抗体类药物。未来篇PD-1/PD-L1掀起了肿瘤治疗领域的新篇章。随着科学家和医务工作者们对于肿瘤机理和药物治疗的不断改进和创新,新的PD-1/PD-L1也将会陆续诞生,并进一步提高肿瘤治疗的疗效和患者生存率以及生活质量。也许,在不远的未来,完全治愈肿瘤疾病将会从梦想变成现实!对于我们中国的老百姓而言,得益于优先审批的绿色通道,Opdivo这款患者急需的PD-1在中国的审批一路畅通,于今年6月批准上市。而仅过了1个月,Keytruda也登陆中国,而且从递交到获批用时不到6个月,创下了中国进口抗肿瘤生物制剂最快审批记录。就获批适应症情况来看,PD-1的使用仍较为受限,Opdivo获批的适应症仅为表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性局部晚期或转移性非小细胞肺癌(NSCLC)成人患。Keytruda目前的适应症为局部晚期或转移性黑色素瘤。除了以上提到的进口药以外,目前至少已经有17个国产的PD-1抑制剂(PD-1抗体、PD-L1抗体)进入临床试验或者即将进入临床试验,有望在1到两年内进入市场。PD-1抑制剂以及其新的适应症会获批的越来越快,也会有更多的肿瘤患者能用得上这类好药。放眼世界的历史长河,早在上世纪50年代,人们就掀起了肿瘤免疫学研究的热潮,2013年,《科学》杂志将免疫治疗列为年度十大科学突破之首,这也让免疫疗法再次成为全球研发的热点。目前除了PD-1抑制剂这一类的单克隆抗体以外,还有细胞治疗(比如最近大火的CAR-T疗法),肿瘤疫苗(如宫颈癌疫苗),小分子抑制剂,免疫系统调节剂等。第二季2018.5.20过去的四五年时间里,在癌症治疗领域有一种新药异军突起、名声大噪,接连被《科学》、美国临床肿瘤学会评选为“年度最大进展”,这种新药就是PD-1抑制剂。在坊间,PD-1甚至被誉为“抗癌神药”,那么PD-1抑制剂到底是什么?它的作用原理是什么?它的有效率又是什么?接下来的15个问题带你读懂PD-1。1.PD-1抑制剂是什么?PD-1抑制剂与传统癌症治疗手段(手术、放疗、化疗)的区别:PD-1抑制剂本身并不能直接杀伤癌细胞,而是通过激活病人自身的免疫系统来抗癌。PD-1抑制剂,包括PD-1抗体和PD-L1抗体,是一种肿瘤免疫治疗新药。PD-1抑制剂,2006年开始做第一项临床试验,2014年9月正式上市,PD-1抑制剂的发明人已经获得了被誉为“诺贝尔医学奖风向标”之称的拉斯克医学奖。医学界普遍预计,该重大发明会在最近的几年内,最终问鼎诺贝尔医学奖。2.上市的PD-1抑制剂有哪些?到目前为止,已有2种PD-1抗体和3种PD-L1抗体在欧美几十个国家上市,这5种PD-1抑制剂分别是:Nivolumab(商品名Opdivo,简称O药);Pembrolizumab(商品名Keytruda,简称K药);Atezolizumab(商品名Tecentriq,简称T药);Avelumab(商品名Bavencio,简称B药);Durvalumab(商品名Imfinzi,简称I药)。到目前为止,已经有2种PD-1抑制剂向中国食品药品监督管理总局提交了上市申请,如果审核顺利,将会在2018年在大陆地区上市。分别是:Nivolumab(商品名Opdivo,简称O药)、信达公司生产的PD-1抗体信迪单抗(曾用名:IBI308)。除此之外,还有十几家国产的PD-1抑制剂,如恒瑞、君实、百济等,正在开展临床试验,排队等着上市。从目前已公布的试验和临床数据来看,上述PD-1抑制剂,疗效和副作用基本相当;因此,病友应该结合具体情况,选择最实惠的药品即可。3.PD-1抑制剂已经批准的适应症有哪些?PD-1抑制剂并不适合所有的癌症,有其相应的使用范围。自2014年9月以来,美国FDA正式批准PD-1抑制剂用于:恶性黑色素瘤、非小细胞肺癌、头颈部肿瘤、霍奇金淋巴瘤、肝癌、胃癌、肾癌、膀胱癌、Merkel细胞癌以及所有微卫星高度不稳定(MSI-H)的实体瘤。此外,PD-1抑制剂在结直肠癌、食管癌、三阴性乳腺癌、鼻咽癌、卵巢癌、宫颈癌、前列腺癌、子宫内膜癌、胶质瘤、神经内分泌肿瘤、恶性间皮瘤、非霍奇金淋巴瘤等其他多种实体瘤的治疗上,显示出了初步的、不错的疗效。4.PD-1抑制剂疗效如何?PD-1的有效率如何呢?实际上,在绝大多数、未经挑选的实体瘤中,单独使用PD-1抑制剂的有效率,其实并不高:10%-30%左右。唯一的例外,是经典型霍奇金淋巴瘤,有效率突破60%以上。既然PD-1抑制剂有效率并不高,那为什么学术界和癌友圈还对它有如此多的褒奖呢?主要的原因是:PD-1抑制剂疗效的持久性。由于免疫系统具有记忆功能,因此一旦PD-1抑制剂起效,其中部分病友实现临床治愈,也就是说五年、十年不复发、不进展、长期生存。一组数据说明了这一现象:在晚期恶性黑色素瘤和晚期非小细胞肺癌的治疗上,PD-1抑制剂将生存率提高了数倍:晚期恶性黑色素瘤的5年生存率从15%左右,提高到了35%上下;而晚期非小细胞肺癌的5年生存率从5%左右,提高到了15%上下!5.如何预测PD-1抑制剂的疗效?在未经选择的实体瘤患者中,PD-1抑制剂的有效率只有10%-30%;如何尽可能筛选出适合PD-1抑制剂的患者呢?目前主要的方法有如下几个:(1)PD-L1表达用病理组织切片,做免疫组化,看肿瘤组织中PD-L1的表达。PD-L1表达越高,有效率越高。PD-L1表达,在肺腺癌、恶性黑色瘤等肿瘤中,格外有用。PD-L1表达超过50%的晚期非小细胞肺癌,可以直接首选单独的PD-1抗体K药治疗,有效率在40%上下。(2)肿瘤基因突变负荷(TMB)检测拿病理组织切片,或者抽血外周血,用基因检测法,测定TMB。一般认为,TMB大于20个突变/Mb,就是TMB高。TMB高的患者,接受PD-1抑制剂治疗的有效率高、生存期长。(3)MSI检测拿病理组织切片,或者抽血外周血,用基因检测法检测MSI(微卫星不稳定性)。MSI-H的消化道肿瘤,有效率可以达到50%左右。MSI检测特别适合消化道肿瘤、子宫内膜癌等患者。(4)肿瘤浸润淋巴细胞(TIL)检测通过免疫组化染色(CD3、CD4、CD8等),可以看出肿瘤组织中是否有较多的淋巴细胞浸润。浸润的淋巴细胞越多,PD-1抑制剂的有效率越高。6.如何通过联合治疗,提高治愈率?除了通过上述指标,把对PD-1抑制剂敏感的人群挑选出来;另外一个解决思路是通过联合治疗,把原来不适合PD-1抑制剂治疗的病人,转化为可以从中获益的人群,这就需要给PD-1抑制剂找一个搭档。目前,PD-1抑制剂主流的搭档有如下7种:(1)联合化疗(2)联合另一个免疫治疗药物(3)联合靶向药(4)联合放疗(5)联合个性化肿瘤疫苗(6)联合溶瘤病毒(7)联合特异性肿瘤免疫细胞治疗警示:PD-1抗体、PD-L1抗体联合EGFR抑制剂、或者联合ALK抑制剂,可能发生致命的副作用。携带EGFR敏感突变的晚期非小细胞肺癌,可以接受众多EGFR抑制剂治疗,比如第一代药物易瑞沙、特罗凯、凯美钠,第二代药物阿法替尼、达克替尼,第三代药物奥西替尼(AZD9291)——这些靶向药的有效率高达70%甚至更高,副作用也不大,是这类患者的治疗首选。同理,携带ALK融合突变、ROS-1融合突变的晚期非小细胞肺癌、间变大B细胞淋巴瘤、小部分胶质瘤、小部分肉瘤患者,可以接受众多的ALK抑制剂治疗,比如第一代药物克唑替尼,第二代药物色瑞替尼、艾乐替尼、布加替尼(AP26113),第三代药物劳拉替尼等——这些靶向药的有效率高达80%甚至更高,副作用也不大,是这类患者的治疗首选。有基因突变的病人是幸运儿,有这么多靶向药了,就别“吃着碗里的,想着锅里的”了;但是,依然有部分病友心心念念免疫治疗,一心想尝试PD-1抑制剂。携带EGFR突变、ALK融合突变的晚期肺癌患者,不适合接受PD-1抑制剂,理由有三点:(1)有效率低,不同研究报道不一样,但一般认为低于5%;(2)副作用大,尤其是发生肺炎、肝炎的风险高;(3)可能爆发进展。副作用大这一条,尤其针对的是那些“贪得无厌”、希望“锦上添花”、大胆尝试PD-1抑制剂联合EGFR抑制剂或者ALK抑制剂的病友:PD-1抗体/PD-L1抗体+EGFR/ALK抑制剂,副作用可能是致命的,大家要格外当心!日前,国际肺癌联盟的官方杂志《JTO》公布了一项数据:13位携带ALK融合突变的初治的晚期非小细胞肺癌,接受PD-1抗体O药联合克唑替尼治疗。结果:5位患者出现了严重的肝毒性,不得不停止治疗;其中2位患者抢救失败去世,而且这两位患者的去世均被认为与治疗导致的肝毒性有关。这项临床试验本来还要招募更多患者,现在不得不紧急叫停。已经入组的13名患者,只有5名患者客观有效,有效率为38%(单独吃克唑替尼,有效率都高于60%)——这真是“偷鸡不成蚀把米”,2位病友甚至付出了生命的代价。无独有偶,2016年生产AZD9291这个神药的阿斯利康公司曾经公开报告过一项小规模临床试验的数据:他们尝试利用AZD9291联合PD-L1抗体Durvalumab(这个药物本身用于预防局部晚期非小细胞肺癌的复发转移非常成功,已经正式上市,详见:PD1联合放疗:三大临床试验数据,全解析)治疗EGFR突变的晚期肺癌,结果:64%初治的患者发生了间质性肺炎,其中不少患者是严重的间质性/免疫性肺炎。虽然,阿斯利康公司并未明说是否出现了致死性的事件,但是这个临床试验也是被紧急叫停。此外,PD-1抗体联合易瑞沙、PD-L1抗体联合易瑞沙的临床试验也都已经开展过,疗效并未增加,而副作用明显增加,目前均已处于不再进一步招募患者的停滞状态。PD-1联合治疗(联合化疗、放疗、IDO抑制剂、抗血管生成靶向药、CTLA-4抗体、溶瘤病毒、改良的白介素等)均已取得了一定的成功。但是这并不代表PD-1抑制剂就是“万金油”,就是“百搭”的,时刻牢记是药三分毒,要咨询相关的行业内专家学者,不要拿自己的生命做实验。7.PD-1抑制剂的副作用如何?总体而言,PD-1抑制剂的的副作用比传统的放化疗要小得多。常见的副作用是类似“流感”样的表现,如发热、乏力、头晕、全身肌肉酸痛、嗜睡等,且发生率在30%左右,只需要针对不同的情况进行相应的处理即可,患者的生活质量能够得到很大的提升。此外,大约5%-10%的患者,会出现严重的免疫相关的炎症反应,如甲状腺炎症(表现为甲亢、甲减、或先甲亢后甲减)、免疫性肺炎、免疫性肠炎、免疫性肝炎、甚至免疫性心肌炎。免疫性炎症需要及时发现、处理到位,如果发现不及时,处理不到位,偶尔发生致命的事故。8.PD-1抑制剂的副作用,如何处理?常见的流感样症状:对症处理即可,比如退烧、止痛、多休息等。皮疹:可以用一点尿素软膏、氢化可的松软膏。甲状腺问题:可以请内分泌科医生会诊。甲亢可以服用抗甲状腺药物,甲减可以补充优甲乐。免疫性炎症,如肺炎、肝炎、肠炎等:需要酌情加上口服或静脉的糖皮质激素,如地塞米松、泼尼松、甲强龙等,对于病情较重的,还需要加上环磷酰胺、霉纷酸脂等免疫抑制剂。发生细胞因子风暴的患者:需要及时使用IL-6抗体,托珠单抗。9.使用PD-1抑制剂,如何评价疗效?对于绝大多数实体瘤(淋巴瘤除外),PD-1抑制剂起效平均时间大约是2-4个月。因此,用药以后,每隔6-8周,复查一次影像学是最标准的。影像学提示肿瘤缩小或者稳定,可以继续用药。如果影像学提示肿瘤增大,但是患者一般情况尚可,可以再用药2-3次,以观后效,因为10%左右的患者会出现“假进展“;如果第二次复查,肿瘤继续增大,那就考虑换药。10.什么是假进展和混合反应?一部分病友,在接受PD-1抑制剂治疗后,先出现肿瘤大小的增大,然后逐步缩小,这就是假进展。如何预测和判断“假进展”?目前主要是通过患者症状变化、肿瘤标志物动态改变、PET-CT上SUV改变、细胞因子IL-8等改变、ctDNA含量的改变等方式综合判断,最准确的方式,是对可疑的病灶进行穿刺活检,如果活检出来全是癌细胞,还是考虑是真进展;如果是大量浸润的淋巴细胞、免疫细胞,高度怀疑是假进展。一部分病友,接受PD-1抑制剂治疗后,身体内一部分病灶缩小,另外一部分病灶增大,这就是混合反应(mixedresponse)。这种情况产生的根本原因是一个病友体内不同部位的病灶,对药物的敏感性不同,也就是所谓的异质性。发生这种情况,需要考虑对增大的病灶加一点局部治疗(介入、射频、粒子植入、放疗),或者联合其他治疗。11.PD-1抑制剂如果起效,到底应该用多久?目前国内外,标准的方案是:手术或同步放化疗后,巩固性、辅助性使用的病友,PD-1抑制剂建议用满1年;而晚期的、全身转移的病友,建议用满2年。然而,越来越多的证据支持,使用PD-1抑制剂满6个月,且肿瘤缩小达到完全缓解、部分缓解(肿瘤缩小超过30%以上)的病友,可以再巩固2-3次后,酌情停药或调整剂量和间隔。12.如何克服PD-1抑制剂耐药?PD-1抑制剂有效的病人,一般疗效持久;然而,目前已经观察到30%左右的患者,出现了疾病的耐药。克服耐药的关键,主要是两点:首先,如果可能,可以通过对新增的或者不断增大的耐药部位,进行穿刺活检和深入的免疫分析,找到耐药的原因,根据原因治疗。比如,有的病人是由于TIM-3、LAG-3或IDO代偿性高表达;那么选择,PD-1抑制剂联合TIM-3抑制剂、LAG-3抗体、IDO抑制剂,就是最好的治疗方案。其次,对于不能明确耐药原因的病友,可以参考本文第六点中列出的联合治疗策略,结合具体病情,选择最佳的联合搭档,逆转耐药,延长生存期;或者,更换为放化疗、介入、射频、粒子植入等传统治疗。13.PD-1抑制剂使用,有哪些注意事项?首先,不建议患者尝试PD-1抑制剂的情况:病情进入终末期、无自主行为能力、卧床不起的患者;有急性细菌感染,尚未控制的患者;做过肝移植、肾移植的患者;有系统性红斑狼疮、白塞病、干燥综合征、血管炎等自身免疫病,尚未控制的患者;携带MDM2扩增、EGFR突变、JAK突变等患者等。其次,使用PD-1抑制剂前,一般建议完善如下检查,基本正常,然后再使用:血常规、肝肾功、电解质、凝血、甲状腺功能,心电图、腹部B超、胸部X线。最后,也是最重要的一点:越来越多的证据支持,PD-1抑制剂这类免疫治疗,应该在患者一般情况比较好,肿瘤负荷比较小的时候,尽早用。目前,PD-1抑制剂已经被批准用于局部晚期恶性黑色素瘤手术后的巩固治疗;PD-1抑制剂用于同步放化疗根治后的非小细胞肺癌的巩固治疗,三期临床试验同样大获成功,生存期提高了数倍。14.PD-1抑制剂的渠道和价格如何?PD-1抑制剂在大陆地区并未上市;根据已经提交在中国上市申请的PD-1抑制剂来看,最快于2018年中下旬可以在中国大陆上市。对于国内患者而言,目前用PD-1抑制剂来治疗肿瘤的最佳的方式是参加免费的临床试验。其次,就是通过跨境医疗,前往香港、澳门、日本、韩国、欧美等地购买PD-1抑制剂或条件允许直接在国外治疗。以一个50kg、标准体重的患者为例,K药的用量是100mg,3周一次,每月的花费大约在3-4万元;O药的用药是150mg,2周一次,每月的花费大约在4-6万左右。可以预见的是PD-1抑制剂在内地正式上市后,价格将大幅度下降,届时将会有更多的患者受益。15.除了PD-1,还有哪些有前景的免疫治疗?肿瘤免疫治疗主要包括如下几类:(1)免疫检查点抑制剂(以PD-1为优秀代表)(2)溶瘤病毒(T-VEC已上市)(3)肿瘤疫苗(4)免疫细胞治疗(5)细胞因子第一季2016.8.18一、什么样的病人最适合使用PD-1抗体?菠菜:PD-1/PD-L1抗体在大部分晚期实体瘤和个别血液肿瘤中显示出良好的安全性和不俗的疗效,单药有效率达到10%~40%。为了更好地预测,到底哪些病人更有可能从这个药物中获益,目前已经提出了一些指标:PD-L1表达状态、MSI、突变频率、肠道菌群等。您怎么看待这些指标对患者的实际意义?将来会不会有更准确的预测指标?教授:因为PD-1/PD-L1抗体的直接靶点是PD-1或PD-L1,PD-L1是最直接的预测指标,和这类药物的作用机理直接相关,预测效果应该是最好的,当然前提是要有科学可靠的检测方法。目前利用肿瘤活检的组织进行PD-L1组化检测,还有一些技术性的问题。PD-L1在肿瘤组织中的表达是散在的,也就是说肿瘤组织的不同位置PD-L1的表达是不一样的;后来我们发现,这是因为T细胞分泌的干扰素会上调PD-L1的表达。活检只拿到一小块组织,染色后只能代表一个很小区域的PD-L1表达状态,无法完整准确地反应整个肿瘤组织的情况,因此可能造成假阴性。解决这个问题,有一个好办法:利用体内影像技术进行PD-L1检测。通过这样的技术,可以观察到肿瘤组织整体的PD-L1表达情况和分布规律,大大提高PD-L1作为疗效预测指标的准确率,已经有人在开发类似的技术,我希望这将为我们带来更精准的疗效预测。目前PD-1抗体已经在很多种肿瘤中都显示出了疗效,到底有多少患者有效呢,下图是菠菜整理的具体数字,至于检测了PD-L1以后。单独计算PD-L1阳性的病人,疗效是多少呢?这篇文章如果阅读人数突破五千,下一篇文章,萝卜给大家整理这个数据。二、PD-1抗体,耐药以后怎么办?菠菜:基于目前有限的临床数据和随访资料,对PD-1/PD-L1抗体有效的患者,有一部分疾病最终还是会进展。那么,对PD-1抗体耐药以后,应该怎么处理?教授:基于黑色素瘤和肺癌的几百例病人的统计,对PD-1抗体有效(PR)的患者,复发的概率在15-20%,相关的结果应该很快就会发表出来;其他的肿瘤,目前尚无足够的数据。复发的患者,可以分为两种:一种是患者用药之后效果很好,停药之后复发,但是再用PD-1抗体还是会有效。在黑色素瘤复发病人里,这一类病人占了50%左右。这类复发患者,并不是真正的耐药。另外一种是耐药性的复发。比如有些患者用药还未停止,已经消退的肿瘤(达到PR标准)又生长起来,但这部分患者的比例较小,还没有引起很多关注。由于PD-1/PD-L1抗体在大多数肿瘤中都显示出了很好的苗头,因此绝大多数药企和研究人员,目前主要的精力都在进行PD-1/PD-L1抗体本身的推广和研究。现在只有少数几个包括我们实验室,正在做相关的研究。已经有证据表明,这部分患者的PD-L1/PD-1还在表达,可能是因为其他免疫逃逸通路代偿性活跃起来了,针对这些新通路的药物,还有很多基础研究和临床试验需要去做,因此还需要一些时间新的靶点比如TIM-3等已经被发现,针对性的新药已经在研究,大家耐心等待。三、PD-1抗体有效的病人,要一直吃下去吗,什么时候可以停药?菠菜:国内外的数据显示,一部分一开始对PD-1/PD-L1抗体敏感的病人,由于副作用或者自身其他原因提前停药。这部分病人的疗效在停药以后似乎又维持了很久,总的生存期似乎不受停药的影响。那么,对于一般的患者,如果治疗有效,服药一定的时间,是否也可以选择停药?教授:到目前为止,PD-1/PD-L1抗体用药时间,并没有一个科学的依据。我们在PD-1/PD-L1抗体的一期临床试验的时候,病人只使用了一次PD-1抗体就有很好的效果,而且持续很长时间。我认为,PD-L1/PD-1这种通路有免疫反应导向作用,而不仅仅是简单的一个负反馈。就好像是一个方向盘一样,阻断抗体只要把方向盘转过来,不仅是消除抑制,还可以把整个免疫反应的方向转型,使之向着清除肿瘤的方向发展。这一点和靶向治疗不同,靶向治疗需要一直用药来阻断或者干扰靶点,因为它不能去掉靶点或者改变整个的方向。为此,科学家们正在开发一套综合性的评价指标,来确定患者的免疫反应方向是否发生了改变。比如患者用药前,肿瘤微环境中有很多抑制性的免疫细胞(Treg,MDSC等)和抑制性的免疫调节分子,我们在临床中发现有些患者在几次用药之后这些抑制性的免疫细胞和分子都减少了,患者的免疫反应很可能已经发生了方向性的改变,这时候或许可以停药。这套综合评价指标一旦研发成功,就可以用来指导用药。四、各种化疗、靶向药、放疗等其他手段,能和PD-1抗体一起用么?菠菜:联合治疗是目前一个热门的话题,手术、放疗、化疗、靶向治疗、免疫治疗,如何有机组合,您怎么看未来的前景?教授:我个人谨慎看待这些联合治疗的手段,因为目前的联合治疗更多的是一些随机的甚至是有些盲目的联合。比如,某药企恰好有个其他什么药,他们希望和热门的PD-1/PD-L1抗体联合,期待能有好的效果。这些联合治疗现在大多是由药物公司在导向,很多都缺乏科学依据。当然,任何新生事物,一开始都是不完美的;就像西部大开发,刚开始的时候大家比较盲目,一窝蜂的去做,抢到一块算一块,到后来,热情冷却下来,渐渐地就会理性地去分析问题,总结经验教训,然后效果就会好很多。目前这种阶段,可能会持续3-5年,等这一批盲目的尝试,该失败的都失败了以后,大家就会更理性地看待联合治疗,然后设计出更合理的临床试验。科学的进展需要很长时间的艰苦探索和点滴积累,不是天上掉馅饼,捡到就可以吃的;中间还有很多的挫折,最终才会有一个理想的结果。科学进步的每一步,从基础研究到临床应用,都需要很长的时间,希望患者能够理解。五、一旦有脑转移,很多药都没用了,PD-1抗体还能用么?菠菜:PD-1抗体早期的临床试验是排除脑转患者的,但是很多患者到了晚期都会面临脑转移的风险,那么PD-1抗体对于脑转移或者脑部原发肿瘤的患者有效吗?教授:我们在做第一个PD-1抗体临床试验的时候,确实是排除了所有脑转移的患者。因为当时大家认为:脑转移的患者进展太快;而且,由于血脑屏障,当时我们认为抗体是很难通过的,效果不一定很好。现在看来当时我们是有些保守了。虽然健康人的血脑屏障是关闭的,抗体药物很难进入。但是,在疾病状态下抗体药物是有可能透过血脑屏障的;原因可能是炎症或其他细胞因子的作用下,血脑屏障被部分打开了,因此PD-1/PD-L1抗体是可以或至少是部分进入脑组织的。现在,专门针对脑肿瘤患者的临床试验已经启动,结果显示,PD-1/PD-L1抗体针对外周肿瘤脑转移和脑部原发肿瘤比如胶质瘤,确实是有效的;具体的结果,很快会发表出来。另外,很多脑转移的患者会进行脑部放疗,放疗和PD-1抗体的联合对于控制脑部肿瘤可能是不错的方法,尤其是针对脑部没有广泛扩散的患者。放疗会损伤一部分肿瘤细胞,造成炎症的产生,还可以帮助开放血脑屏障,已经有一部分的试验数据支持这种理论。所以,脑部肿瘤如果能做局部放疗,对PD-1/PD-L1抗体是有帮助的;这也是美国前总统卡特的疗法:先脑部局部放疗,然后结合PD-1抗体控制脑部肿瘤进展。这是未来很有前景的治疗方案。PD-1抗体和放疗联合,应用于脑转移的患者,不仅陈教授很看好,事实上,也有喜人的数据作支持。上个月,一项纳入了26名恶性黑色素瘤脑转移的患者临床研究显示,同时使用放疗和PD-1抗体,脑部肿瘤1年的控制率在85%,且联合治疗的安全性很好,只有1例患者出现了2级的头痛(参考文献:AhmedKA,StallworthDG,KimY,etal.Clinicaloutcomesofmelanomabrainmetastasestreatedwithstereotacticradiationandanti-PD-1therapy.AnnOncol.2016;27(3):434-41)。六、癌症还处于早期,或者是做完手术担心复发,能用PD-1抗体么?菠菜:目前PD-1/PD-L1抗体仅被FDA批准用于各种“标准疗法”失败的晚期患者,也就是用于二线三线或最后的治疗手段。它们有没有潜力被用于一线治疗晚期患者,甚至用于治疗早期肿瘤?教授:目前PD-1抗体用于常规治疗手段失败的晚期患者,这是新的疗法都会经历的阶段,毕竟临床试验的开展需要符合伦理学的基本要求。但是PD-1/PD-L1抗体已经开始用于一线治疗晚期肺癌,而且证明疗效要比二线用药好很多。原理其实很简单:许多化疗药都会损伤免疫细胞。现在的趋势很清楚,PD-1/PD-L1抗体会很快在部分病人里代替化疗,特别是PD-L1阳性的病人。治疗早期肿瘤肯定会是将来的方向。我们的研究发现,早期患者(一期或二期)没有经过一系列对免疫系统有损伤的常规治疗,免疫系统更健康。因此可以预测,他们使用PD-1/PD-L1抗体的效果可能会更好。PD-1抗体应用于更早期的患者或许效果更好,事实上也是有类似的临床数据的。去年有一项相关的临床研究。33例恶性黑色素瘤患者在手术后,接受了PD-1抗体和靶向HMB-45、NY-ESO-1和MART-1的肿瘤疫苗联合治疗,平均随访了32.1个月,23个患者仍然未复发,平均无复发生存时间大约是47.1个月,而平均总生存期尚未达到(参考文献:GibneyGT,KudchadkarRR,DeContiRC,etal.Safety,correlativemarkers,andclinicalresultsofadjuvantnivolumabincombinationwithvaccineinresectedhigh-riskmetastaticmelanoma.ClinCancerRes.2015;21(4):712-20)。七、除PD-1抗体外,免疫治疗还有很多种,如何评价细胞治疗、生物治疗呢?菠菜:肿瘤免疫治疗,除了PD-1/PD-L1抗体,还有其他方式,比如CAR-T等。您怎么看待这些新疗法的前景?教授:从现在来看,其他的肿瘤免疫治疗手段并不具备像PD-1/PD-L1抗体一样的广谱性。比如CAR-T在实体瘤里,还没有任何的证据证明可以治好实体瘤,在血液瘤中也仅限于非常小的人群,事实上到目前为止,仅限于CD19这个靶点有显著疗效,换一个靶点的效果,都没有那么好。这个疗法到底是有普遍意义,还是仅限于个别疾病,还有待研究。我认为现在这个疗法炒作得有点过热了。在细胞治疗领域里,TCR-T已经有治疗多种实体瘤的记录,应该有比CAR-T有更好的广谱性。问题是制备过程复杂,费用昂贵。至于国内曾经一度开展的很火热的生物治疗、细胞治疗,其实主要是CIK、DC-CIK等尚未有充分证据支持的、欧美主流医学界已经不再提及和关注的旧技术。2016年5月4号,国家卫计委已经全面叫停了上述细胞治疗手段应用于临床,并收取昂贵费用的行为。请各位咚友擦亮眼睛,不要上当受骗!
 李鉴 主任医师 医科院肿瘤医院 胸外科6.1万人已读
李鉴 主任医师 医科院肿瘤医院 胸外科6.1万人已读 - 精选 尿道粘膜脱垂prolapseofurethra
概述:尿道粘膜脱垂又称尿道粘膜外翻,是指尿道黏膜呈一半环形或环形的肿块脱出外翻于尿道口外,其呈紫红色、触到有痛感,易出血。名发生于5-14岁女性儿童及绝经期妇女。比较罕见。无论是幼儿还是成人患者,只要黏膜脱出,就应该立即复位。如果脱出时间长,脱垂组织充血、水肿严重,应前往医院就诊,尽可能请医生手法复位。病因:发病机制尚不清楚,但与下列因素有关:先天性或后天性损伤所致尿道周围支持组织缺陷;绝经期妇女雌激素水平下降;膀胱及尿道压增高;因咳嗽、便秘等因素所致腹压增高。儿童患者:由于儿童尿道黏膜脱垂见于体弱的女孩,所以一般认为本病症的发生与骨盆快速增大、盆腔器官发生变化有一定的联系,若尿生殖膈薄弱、尿道黏膜与黏膜下黏合的先天性缺损,更易发生黏膜脱垂。老年妇女:尿道黏膜脱垂可能是由于分娩损伤、绝经后雌激素水平降低,尿道周围组织萎缩、或全身衰弱等所致的尿道壁薄弱、尿道周围组织松弛以致尿道黏膜翻出。其他:如剧烈咳嗽、便秘、腹泻、分娩、尿路感染、负重等使膀胱压力过高,造成膀胱尿道压力不平衡,加之尿道周围支持组织力量不足,也可导致本病的发生。其他如膀胱结石、尿道结石或肿瘤的直接压迫也可诱发。临床表现症状:患者有尿频、尿急、排尿痛,偶伴有出血等下尿路刺激症状。1.尿频、尿急:轻者常有局部灼痛感并有尿频和尿痛和排尿疼痛等尿路刺激症状,宛似尿道肉阜的症状。2.尿道出血:活动后发现尿道口处出血,量或多或少。3.尿道口肿块:可见环形或半环形紫红色肿块脱出,尿道口位于肿块中央,插入导尿管见有尿液流出。重者也可伴有感染、糜烂、片状坏死或有脓苔黏附、有血性浆液性分泌物及臭味。由于血栓形成、组织坏死,导致剧烈疼痛。查体:位于尿道口的肿物,部分性脱垂者肿物位于尿道口后侧(6点处),完全性脱垂者黏膜呈环状脱出,而尿道口则位于肿物中央,肿物直径为1~5cm,颜色由鲜红转为暗红乃至青紫色,常伴有浆液血性渗出液。治疗1.保守治疗对幼儿患者,大多数可以自愈。因此,这类患儿以非手术治疗为主。对于行经前女孩、轻度黏膜脱垂者,可先采用保守治疗。可采用抗生素,局部涂雌激素油膏及热水坐浴。绝经期妇女可口服雌激素,并行脱垂复位。2.手术治疗适用于保守治疗无效、黏膜脱垂明显者,尤其嵌顿性脱垂者。成人不完全脱垂可用注射疗法,而完全型脱垂的治疗以手术为主,但术后并发症较多。1.环形切除:是最常用的手术方法。将尿道黏膜与前庭黏膜缝合,以防止尿道外口狭窄。但应注意切除时勿用力向外牵拉尿道黏膜,以免切除过多!如果粘膜完全脱垂,通常水肿较重,管腔可能不明显。此时可以抓住脱垂的粘膜,轻轻地将其拉向术者。仔细切开周围的脱垂粘膜,并将其除去,使正常的非水肿性尿道粘膜在外部尿道口内可见。2.环扎术:一般较少用。尿道内置一导尿管,在脱出黏膜的基底部用4号丝线缚扎于导尿管上,让其坏死脱落。3.放射式电凝在脱垂的黏膜四周做放射式电凝,每两周1次,数次后因纤维化而回缩。
赵伟 主任医师 聊城市人民医院 泌尿外科2322人已读 - 精选 「精液带血」,在家先给自己做个初步诊断
出血,对于生育期的女性来说,是稀松平常的事儿,几乎每个月都会来那么一次,没什么大惊小怪的;然而,放到男人身上,那就不得了,精液是男性传宗接代的“使者”,试想一下,一个成年男性,平时每次性活动射出来的都是乳白色的“牛奶”,如若突然有一次竟然射出来“牛奶”变了色,带了血,甚至出血日久量多的话精液还会变成“酱油”色,直接可能吓尿了!!!医学上我们称这样的问题为“血精”,它是男性生殖系统多种疾病引起的常见症状。今天我将为你详细解答有关“血精”的来龙去脉,重点解答以下患者经常问及的问题: 热点问题:1.到底什么是“血精”?2.引起“血精”的原因有哪些?3.患者出现“血精”后会给健康带来什么不良反应?4.什么情况下会诱发患者出现“血精”?5.是不是所有的“血精”患者都要就医?如何就医?6.出现“血精”对患者以后的生活有什么深远的影响吗?一、什么是“血精”?血精,顾名思义就是精液中带有血液,是泌尿外科和男科门诊一种常见症状,好发于年龄小于40岁的中青年男性。根据【病变性质不同】及【含血量的多少】可以表现为:(1)肉眼血精,多见;(2)镜下血精,常于体检时发现。根据【好坏不同】可以分为:(1)好的血精:绝大多数情况下,血精是一种无痛的、良性的、自限性疾病;(2)坏的血精:血精可能是泌尿男性生殖系某些肿瘤的首发症状,如前列腺癌、膀胱癌、睾丸肿瘤等。二、“血精”的常见病因有哪些?(一)无需特殊治疗的病因:不良习惯引起“血精”1、不良“日常生活”方式:过度饮酒,辛辣食物刺激等因素也可诱发血精;2、不良“性生活”方式:精囊的主要生理功能为贮藏精子和分泌精囊液,同时精囊内壁分布许多微小血管,这种结构极易因充血、过度充盈和损伤等因素导致出血。比如过高强度、过长时间的性刺激且同时控制射精久而不射,过于频繁的性生活皆可导致血精;主要是因为精液长期滞留于精囊内,使精囊过度充盈,挤压使精囊膨胀充血,或者在性生活过程中,由于射精时平滑肌的猛烈收缩,导致精囊内壁的小血管破裂而使红细胞从血管内漏出,积聚于精囊内,从而使射精时出现精液中带有血液。通常此类情况无需特别治疗,可通过调节生活方式和改善性生活节律而达到缓解症状的目的。(二)需治疗的病因:泌尿生殖道炎症或感染,医源性损伤,梗阻,生殖道囊肿,新生物和前列腺部尿道的血管异常等1、感染或炎症是最多见的病因常见的70%“血精”患者系感染所致,感染后炎症过程可刺激局部管道系统粘膜充血、水肿并导致出血,比如精囊炎、前列腺炎、泌尿道感染、直肠炎症等皆可导致器官紧密相邻。其中大多数青年“血精”患者的病因是炎症与感染,以精囊炎及前列腺炎最多见。感染多数为非特异性细菌感染,但淋球菌、结核分支杆菌、病毒、衣原体、支原体及寄生虫感染等均可以引起“血精”。2、医源性损伤:手术和有创检查前列腺穿刺活检、膀胱尿道镜检查、尿道扩张术、经尿道前列腺电切术等损伤性操作,可能伤及前列腺,精囊或射精管区域,导致一过性或暂时性“血精”。3、射精管梗阻或囊肿射精管梗阻后可使梗阻的近端管道扩张和膨胀,导致粘膜血管破裂、出血。导致射精管梗阻的原因可以是局部炎症、感染,也可以是射精管区域的囊肿压迫,如常见的前列腺小囊囊肿和苗勒氏管囊肿。4、生殖系统相关肿瘤:以40岁男性为界各种良性肿瘤如尿道中的异位前列腺组织、前列腺息肉和增生性尿道炎等可以引起血精,前列腺、睾丸和精囊的恶性肿瘤也可以引起“血精”。对于长期顽固的血精患者,需要考虑到这类肿瘤的可能性,需进行相关检查排除。一般认为40岁以下的男性患者中,血精多趋向于良性病因,肿瘤的可能性极小。而对于年龄大于40岁的男性患者,则需要考虑或排除恶性病变的可能性,这类患者应进行适当的相应检查,排除泌尿生殖系肿瘤。5、血管异常精囊、前列腺部尿道和膀胱颈部的静脉曲张、动静脉畸形、血管瘤可以导致血尿及“血精”。6、全身性因素一些全身系统的疾病也会造成“血精”的局部表现,如高血压、血液系统疾病、肝脏疾病等。临床上也见到不少因为放了心脏支架(或做了搭桥)需要长期服用抗凝药“华法令”而出现的“血精”。三、“血精”患者有哪些临床症状?单纯的“血精”患者一般无明显的其它自觉不适症状,“血精”持续时间一般从几个星期到几个月不等。很多患者表现为自限性,即出现“血精”数次后自然消失。大约有57%血精患者于发病后1月自然缓解。 1、主要症状:会阴部不适、胀痛或剧痛,疼痛可向生殖器、腰骶部、下腹部、腹股沟部放射。2、全身症状:常有畏寒、发热、头痛、全身乏力等。3、精路症状:性交时,出现肉眼血精,伴有射精疼痛,向会阴、下腹、睾丸放射。4、尿路症状:因后尿道常同时受累,故可出现尿道烧灼感、尿频、尿急、尿痛、终末血尿、排尿困难等。5、性功能障碍症状:如早泄、遗精、勃起功能障碍。四、“血精”患者需要行哪些检查来明确病因?1、经直肠B超 (TRUS)是一种安全、价廉、无创且无辐射的检查手段,能初步筛查血精的病因,并可观察前列腺、射精管、输精管壶腹部及精囊区域的形态和结构的改变,能检出该区域有无结石,并能准确判断如息肉或肿瘤等软组织肿块,可初步明确血精的原因及部位,是血精患者的首选影像学检查。2、磁共振(MRI)当经B超检查不满意或不能明确诊断时,尤其是血精症状反复发作的顽固性血精症患者,选择磁共振MRI检查则具有重要意义,MRI的独到之处在于能更精确地显示前列腺、射精管、输精管壶腹及精囊多层面解剖图像,并能清晰地显示该区域的结构变化和精囊内信号强度的改变,同时,MRI还对前列腺癌的分期具有重要的参考价值。因此被认为是男性性腺、附属性腺及其导管影像学检查的金标准。在临床上,某些经过长期的药物保守治疗症状仍然反复发作的顽固性血精患者,尤其是同时伴随有血尿、射精痛、不育症、其它下尿路症状、不能排除肿瘤等病理性改变的40岁以上患者,需进一步进行上述影像学检查来明确病因。五、“血精”需要治疗吗?保守治疗有哪些?1、良性的、自限性“血精”临床上大多数“血精”患者表现为一种良性的、自限性过程,常常在发作数周到数月内可自行消失。如有的患者在进食大量辛辣食物,连续进食火锅,大量饮酒后出现血精,往往与这类诱因有明确的关系,此种情况,主要需要通过调节生活习惯,消除诱因,往往可自然恢复。治疗方案:以消除患者的顾虑为主,多数无需特殊治疗,这种偶发的血精患者,可以观察等待。2、顽固性“血精”有不少“血精”患者,无明显诱因出现反复,称之为“顽固性血精”,甚至通过各种药物治疗均无效,这类情况常常引起患者的极度紧张和焦虑,此时,应该进行相应的必要检查,以查明确切的病因,并根据病因、病灶部位及病变性质而采取针对性和个体化方法治疗。 (1)明确病因:首先通过详细的病史询问、全面体检,精液或前列腺液常规分析、前列腺精囊B超或磁共振等,首先鉴别是“肿瘤性”还是“非肿瘤性”的。治疗原则:1)肿瘤性:针对病因进一步检查和治疗,这里不做具体阐述;2)非肿瘤性:根据前列腺液或精液细菌培养的结果,分为感染性和非感染性。(2)感染性“血精”:予以“抗生素+安络血+维生素C”口服外,还嘱咐药物治疗期间进行规律的性生活(使用避孕套),每周性交(或手淫)2~3次,对于因为勃起困难不能按照医嘱完成者给予PDE5抑制剂辅助治疗。对于感染性血精症患者,在治疗疗程结束后,经前列腺常规和精液白细胞计数已经恢复正常但仍有血精者,在继续药物治疗的同时,嘱予以禁欲(同非感染组),并继续治疗1个疗程。(3)非感染性“血精”:予以“安络血+维生素C”口服,并嘱咐患者在治疗期间予以适当禁欲,每半月性生活一次。治疗一个月为一个疗程。请注意:所有患者在治疗期间避免无射精活动的性刺激!六、(推荐)精道内镜--“精囊镜”:集“诊断与治疗”的不二之选经药物保守治疗1月以上无效或血精症状反复或持续发作超过3-6个月者称为顽固性血精,对于顽固性血精患者的治疗,目前精道内镜—“精囊镜”是制服“血精”的有力武器,它是一项使用内窥镜行精道疾病诊治的技术,顾名思义,精道内镜就是逆行沿着男性精液射出的途径进入到男性精道中,观察疾病病因并对因治疗的一种手术方式,说的再通俗点,就是精液怎么射出来的,我就沿着这条路去找,能直观、准确发现病变,看看血是从哪里出来的,并具有良好的手术效果。图一:我科常规开展“精囊镜”治疗(1)安全方面:不开刀,不打洞,精囊镜从病人的尿道外口(尿尿的地方)进入,不过不用担心,这个内镜非常细,对尿道几乎没有损伤;(2)治疗方面:精囊镜不但可以直观的观查精囊以及精道,还可以进行相应治疗,比如说发现是炎症导致的出血,可以直接在内镜下利用激光烧灼止血。如果是精道结石堵塞引起的出血,可以利用套石篮将结石取出。如果是良性息肉或比较小的肿瘤,可以直接取病理活检并利用激光烧灼肿瘤。(3)手术相关问题:★★★★☆1)手术适应证(适合哪些人):顽固性血精,经常规保守治疗无效者;2)手术禁忌证(哪些人不能做):①全身功能较差不能耐受手术者;②严重的泌尿系感染未得到有效控制者;③未排除由恶性疾病造成的顽固性或复发性血精。七、“血精”对患者的远期影响如何?1、明确病因的“血精”都是可以得到有效治疗由于导致血精的病因多为良性病变,故无论是偶发的血精,还是顽固性血精,对大部分患者而言,其对患者的远期健康影响均不大。但对于血精患者进行长期的随访观察仍是必要的。通过药物保守治疗后血精能够消失的大部分患者一般可解除顾虑,无需进行特别的治疗,但对药物保守治疗效果欠佳,尤其是对于血精症状反复、有家族史及年龄大于40岁者有必要全面检查以排除肿瘤的可能,通过上述影像学检查及微创手术治疗,一般均可明确病因,排除肿瘤,并能达到彻底治愈的效果。2、另外“血精”对【生育的危害】主要有以下几个方面:(1)精子战斗力下降:血精时精浆成分的改变,精浆酸性物质增加,使精液的PH值由平时适于精子存活的弱碱性,下降至精子最低存活要求的6以下,精子活力下降,甚至死亡;(2)射精管堵塞,梗阻性无精子症:精囊腺位置深在,不容易达到有效的药物浓度,反复发作易转为慢性精囊炎,甚至引起继发性射精管阻塞,导致精液无法排出;(3)血精时,精浆粘稠度会显著增加,导致精液感染,迟缓液化。八、血精患者的饮食、生活需要注意哪些方面?1、平时要养成良好的饮食和生活习惯,避免久坐和憋尿,注意加强体育锻炼,增强体质,提高机体抵抗能力;2、预防感冒,积极治疗全身可能存在的感染,尤其是泌尿生殖系统的感染,中青年患者主要注意预防和积极治疗慢性前列腺炎,精囊炎;3、清淡饮食,少食辛辣刺激食物和酗酒;4、适度规律的性生活。嘉兴地区患者如需预约检查或手术点击https://zhanggaoyue1122.haodf.com进入我个人工作室选择图文咨询或电话咨询!
张高岳 主治医师 上海计生所医院 男科3674人已读 - 精选 前列腺癌诊疗指南-激素非依赖性前列腺癌治疗
六、激素非依赖性前列腺癌治疗 (一)激素非依赖(hormone independent)前列腺癌的概念 1.经过持续内分泌治疗后病变复发、进展的前列腺癌,包括雄激素非依赖性前列腺癌(androgen-independent prostate cancer,AIPC)和激素治性前列腺癌[1-2] (hormone-refractory prostate cancer,HRPC)。 内分泌治疗是目前前列腺癌的主要治疗方法,大多数患者起初都对内分泌治疗有效,但经过中位时间14~30个月后,几乎所有患者病变都将逐渐发展为激素非依 赖前列腺癌。在激素非依赖发生的早期有些患者对二线内分泌治疗仍有效,称为雄激素非依赖性前列腺癌(AIPC),而对二线内分泌治疗无效或二线内分泌治疗 过程中病变继续发展的则称为激素难治性前列腺癌(HRPC)。 2.HRPC定义[1-2] 1)血清睾酮达去势水平(50%,平均有效时间为4~6个月[7]。 (2)停用抗雄激素药物:对于采用联合雄激素阻断治疗的患者,推荐停用抗雄激素药物,停用4~6周后,约1/3的患者出现“抗雄激素撤除综合征”,PSA下降>50%,平均有效时间4个月[8]。 (3)抗雄激素药物互换:氟他胺与比卡鲁胺相替换,少数病人仍有效。 (4)肾上腺雄激素抑制剂:如酮康唑,氨基苯乙哌啶酮,皮质激素(氢化可的松、强的松、地塞米松)。 (5)低剂量的雌激素药物:雌二醇,甲地孕酮等。 3.化学治疗 对于激素难治性前列腺癌(HRPC)目前有以下化疗方案可供选择: (1)以docetaxel(多烯紫杉醇)为基础的化疗方案:docetaxel 75mg/m2,每3周1次,静脉用药,加用强的松5mg,2次/日,口服,共10个周期[9,10]。 (2)以mitoxantrone(米托蒽醌)为基础的化疗方案:mitoxantrone(米托葸醌)12mg/m2,每3周一次,静脉用药,同时联合强的松治疗,可在一定程度控制疾病进展,提高生活质量,特别是减轻疼痛[11]。 (3)其他可选择的化疗方案有: estramustin(雌二醇氮芥)+vinblastine(长春花碱) [12] estramustin(雌二醇氮芥)+etoposide(VPl6) [13] (四)激素非依赖前列腺癌的骨转移治疗 对于有骨转移的激素非依赖前列腺癌的治疗目的主要是缓解骨痛、预防和降低骨相关事件(skeletal related events,SREs)的发生,提高生活质量,提高生存率。骨相关事件包括:①病理性骨折;②脊髓压迫;③为了缓解骨骼疼痛,预防、治疗病理性骨折或脊 髓压迫而进行的放疗;④骨骼手术;⑤为了治疗骨痛而改变抗癌方案;⑥恶性肿瘤所致的高钙血症(hypercalcemia) [14-17]。 1.双磷酸盐(zoledronic acid,唑来磷酸) 唑来磷酸是第三代双磷酸盐,具有持续缓解骨痛,降低骨相关事件的发生率,延缓骨并发症发生的时间。是目前治疗和预防激素非依赖前列腺癌骨转移的首选方法 [15]。推荐剂量:唑来磷酸4mg,静脉15分钟滴注,每4周一次。为了避免药物对肾功能的损害,静脉滴注时间不少于15分钟。研究证明,唑来磷酸 4mg,15分钟静脉滴注对肾功能无明显影响,与安慰剂比较无显著差异。 2.放射治疗 体外放射治疗可改善局部和弥漫性骨痛。因前列腺癌患者发生多处骨转移的机会较高,因此体外放射治疗的范围和剂量越大,副反应越大。放射性核素在前列腺癌骨 转移导致的多灶性骨痛的治疗有一定疗效。89锶和153钐是常用的放射性核素,89锶比153钐发出的β-射线能量高,但半衰期短。Ⅲ期临床研究显示单独 应用89锶或153钐可以显著减少新发骨转移灶,降低骨痛症状,减少止痛药用量[18]。最常见的副反应为骨髓抑制。 3.镇痛药物治疗 世界卫生组织(WHO)已经制定了疼痛治疗指南,也适用于前列腺癌骨转移患者。镇痛治疗必须符合这一指南,规律服药(以预防疼痛),按阶梯服药:从非阿片 类药物至弱阿片类,再至强阿片类药物的逐级上升,还要进行适当的辅助治疗(包括神经抑制剂、放疗、化疗、手术等)。
邢东亮 副主任医师 郑大五附院 泌尿外科5595人已读 - 医学科普 肾盂肿瘤、肾盂癌不要怕
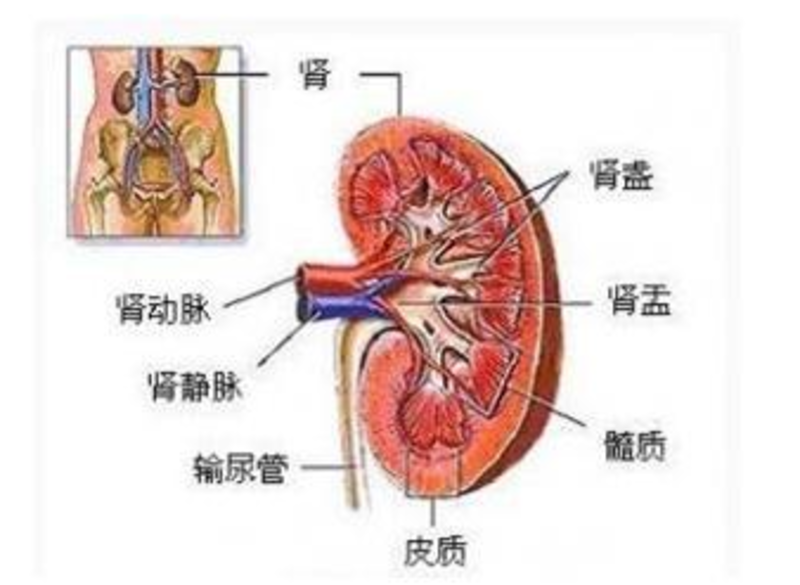
(患者)肾盂癌是什么? ——(医生)顾名思义咯,肾盂癌就是肾盂发生的癌,癌就是癌症,是恶性肿瘤。 (患者)肾盂在哪里? ——(医生)肾盂在肾脏里,肾脏外面一层叫肾脏皮质,就是咱们吃的那个“火爆腰花”,腰花就是把肾脏皮质切了花刀喔。肾脏皮质下面有肾盂,请看图(附肾脏剖面解剖图)。 (患者)一个肾脏原来还分肾皮质和肾盂呀! ——(医生)肾皮质发生的恶性肿瘤属于肾癌,全称是肾细胞癌;而肾盂里发生的恶性肿瘤是肾盂癌,属于尿路上皮癌的一种,和肾细胞癌科不是一个类型。肾癌和肾盂癌别看一字之差,其实完全是两个疾病,不可混为一谈哟。 (患者)肾盂癌是怎么得上的呢? ——(医生)肾盂癌的发生是一个多因素多阶段的过程。抽烟喝酒等不良生活习惯、染料油漆等化工制品都是诱发因素之一。而且,现代基因组学研究发现,大多数的恶性肿瘤患者体内都存在着某些基因的异常改变,一些平时沉默的致癌基因被激活、另一些平时起作用的抑癌基因失去活性,还有一些基因发生了缺失或突变,综合在一起,就生病了。 (患者)得了肾盂癌要怎么治疗呢? ——(医生)肾盂癌的治疗是以手术为主的综合治疗,其中手术切除患侧肾、输尿管和(或)部分膀胱是最关键的治疗,术后医生会根据不同患者的个体情况,在推荐一些化疗、放疗、生物治疗、综合免疫治疗等等,不同的患者不同情况,具体听医生的。
 张运召 副主任医师 威海市立医院 泌尿外科8470人已读
张运召 副主任医师 威海市立医院 泌尿外科8470人已读